Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
- Phương trình điện phân:
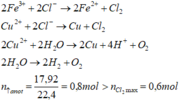
Chứng tỏ anot đã có O2 thoát ra
⇒ n O 2 = 0 , 8 - 0 , 6 = 0 , 2 mol Có 2 n Cl 2 + 4 n O 2 = 2 . 0 , 6 + 4 . 0 , 2 > 0 , 4 + 2 . 0 , 6 = n Fe 3 + + 2 n Cu 2 +
=> Chứng tỏ Cu2+ đã bị điện phân hết, ở catot H+ đã bị điện phân (H+ sinh ra ở anot, di chuyển về catot)
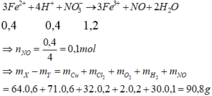
Gần với giá trị 91 nhất

Đáp án D
nFe3+ = 0,08 (mol); H+ còn dư
Dd Y gồm: FeCl3 , FeCl2, CuCl2, HCl dư
Qúa trình điện phân dd Y
Catôt (Fe3+, Fe2+, Cu2+, H+) Anốt (Cl-)
Fe3+ +1e → Fe2+ 2Cl- + 2e → Cl2
0,08 → 0,08
Cu 2+ + 2e → Cu
x → 2x
2H+ + 2e → H2
Khi catốt có khí thì ngừng => chưa xảy ra phản ứng điện phân H+
Gọi nCuCl2 = x (mol)
=> ne trao đổi = 0,08 + 2x = 2nCl2
mdd giảm = mCu + mCl2 = 64x + 71( 0,04 + x) = 13,64
=> x = 0,08 (mol)
Gọi số mol Fe3O4 và Fe2O3 lần lượt là a và b mol
BTKL: 232a + 160b + 0,08.64 = 27,2 (1)
2Fe3+ + Cu → Fe2+ + Cu2+
=> nFe3+ sau = nFe3+ ban đầu – nCu
<=> 2a + 2b – 2.0,08 = 0,08 (2)
Từ (1) và (2) => a = 0,04 ; b = 0,08 mol
BTNT Fe: nFe2+ = nFe bđ – nFe3+ sau = 0,2 mol
nH+ dư = nHCl dư = nHCl bđ – 3nFeCl3 – 2nFeCl2 – 2nCuCl2 = 0,1 mol
Sau điện phân thì nFe2+ = 0,28 (mol); nCl- = 0,66 (mol); nH+ = 0,1 (mol)
Khi cho AgNO3 vào:
3Fe2+ + 4H+ + NO3- →3Fe3+ + NO + H2O
0,075← 0,1
Ag+ + Fe2+ → Fe3+ + Ag↓
(0,28 – 0,075)→ 0,205
Ag+ + Cl- → AgCl↓
0,66 → 0,66
m↓ = mAg + mAgCl = 0,205.108 + 0,66.143,5 = 116,85(g)

Đáp án A
I = 2,68 A; t = 6h ; nKhí = 4,48/22,4 = 0,2 (mol)
![]()
Tại catot xảy ra quá trình oxi hóa Cu2+ Tại anot xảy ra quá trình oxi hóa Cl-, H2O
Cu2+ +2e → Cu 2Cl- → Cl2 + 2e
a → 0,5a → 2a (mol)
2H2O → O2 + 4H+ + 4e
b → 0,5b → 2b → 2b (mol)
Vì dung dịch sau phản ứng tác dụng được với Fe và rắn thu được gồm 2 kim loại => Cu2+ còn dư sau quá trình điện phân. Và có khí NO thoát ra => tại anot H2O bị điện phân để sinh ra H+
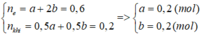
=> nH+ = 2b = 0,4 (mol)
Vì Fe dư sau phản ứng nên Fe chỉ lên số oxi hóa +2; gọi số mol Cu2+ dư là x (mol)
3Fe + 8H+ + 2NO3- → 3Fe2+ + 2NO + 4H2O
0,15 ← 0,4 (mol)
Fe + Cu2+ → Fe2+ + Cu↓
x ← x → x (mol)
Khối lượng kim loại giảm: ∆ giảm = mFe phản ứng – mCu sinh ra
=> (20 – 12,4) = 0,15 + x).56 – 64x
=> x = 0,1 (mol)
=> nCu2+ bđ = nCu2+ đp + nCu2+ dư = 0,6/2 + 0,1 = 0,4 (mol)
=> m = mCu(NO3)2 + mNaCl = 0,4. 188 + 0,2. 58,5 = 86,9 (g)

Quy hỗn hợp thành Fe2O3, FeO và CuO với số mol lần lượt là a b và c.
Ta có sơ đồ phản ứng:
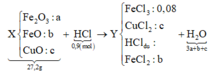
Khi điện phân dung dịch Y đến khi catot thoát khí ⇒ FeCl3 và CuCl2 đã bị điện phân hết.
⇒ mGiảm = nFeCl3×35,5 + nCuCl2×135 = 13,64 gam Û nCuCl2 = 0,08 mol.

●Tóm lại sau điện phân dung dịch chứa: nFeCl2 = 0,28 mol và nHCl = 0,1 mol.
Cho dung dịch sau điện phân + AgNO3 ⇒ 3Fe2+ + 4H+ + NO3– → Fe3+ + NO + 2H2O.
⇒ nFe2+ bị mất đi = 0,1 × 3 ÷ 4 = 0,075 mol
⇒ nFe2+ còn lại = 0,28 – 0,075 = 0,205 mol.
⇒ nAg = nFe2+ = 0,205 mol
nAgCl = nCl– = 0,28×2 + 0,1 = mol.
⇒ m↓ = mAg + mAgCl = 0,205×108 + 0,66×143,5 = 116,85
Đáp án A

Chọn A.
Tại thời điểm t (s) tại anot thu được khí Cl2 (0,05 mol) Þ ne (1) = 0,1 mol
Tại thời điểm 3,5t (s) tại anot có:
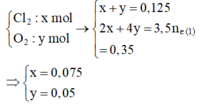
![]() và dung dịch Y chứa Cu2+ dư (a mol), H+ (0,2 mol), NO3-, K+
và dung dịch Y chứa Cu2+ dư (a mol), H+ (0,2 mol), NO3-, K+
Khi cho Y tác dụng với Fe thì: nFe pư =
= 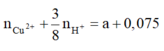
Chất rắn thu được gồm Fe dư và Cu Þ 20 – 56.(a + 0,075) + 64a = 16,4 Þ a = 0,075
Vậy dung dịch X gồm Cu(NO3)2 (0,25 mol) và KCl (0,15 mol) Þ m = 58,175 (g).

Chọn đáp án B
- Ta có
n e t r a o đ ổ i = I t 96500 = 0 , 44 m o l
Quá trình điện phân xảy ra như sau:
| Tại anot |
Tại catot |
| C u 2 + + 2 e → C u 0 , 15 0 , 3 0 , 15 2 H 2 O + 2 e → 2 O H - + H 2 0 , 08 0 , 04 |
2 C l - → C l 2 + 2 e x → 2 x H 2 O → 4 H + + 4 e + O 2 4 x → y |
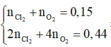

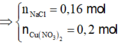
- Dung dịch sau điện phân chứa
![]()
+ Xét dung dịch sau điện phân có:
![]()
mol
- Cho m gam Fe tác dụng với dung dịch trên thì:
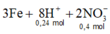
![]()
+ Theo đề ta có: m F e - m r ắ n k h ô n g tan = m F e tan
=> m - 0,8m = 0,09.56 => m = 25,2 (g)


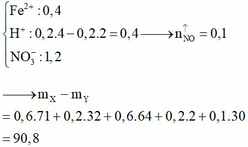

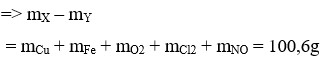


Chọn A.
Tại anot có khí Cl2 và O2 thoát ra với
Tại catot lúc này có:
Dung dịch còn lại sau khi lấy catot ra khỏi bình điện phân chứa Fe2+ dư (0,2 mol); H+ (0,8 mol); NO3– (1,2 mol), lúc này tiếp tục xảy ra phản ứng oxi hóa khử nên n H + dư = 0,8 – 4 3 n F e 2 + = 8/15 mol
Dung dịch Y chứa Fe3+ (0,2 mol); H+ dư (8/15 mol) và NO3– (1,2 mol). Vậy ( m Y - m X = 9 , 67 )