Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi số mol của Al và Fe lần lượt là a và b
Ta có 1,5a + b = 0,25
1,5a = 0,15
=> a = 0,1 và b = 0,1
=> %Al = 32,53%
%Fe= 67,47%

- TN2: m chất rắn = mMg = 0,6 (g)
- TN1: \(n_{H_2}=\dfrac{1,568}{22,4}=0,07\left(mol\right)\)
PT: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
Ta có: \(n_{Mg}=\dfrac{0,6}{24}=0,025\left(mol\right)\)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}+n_{Mg}\Rightarrow n_{Al}=0,03\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,6}{0,6+0,03.27}.100\%\approx42,55\%\\\%m_{Al}\approx57,45\%\end{matrix}\right.\)

* TN2:
Chỉ có Al tác dụng với dung dịch NaOH và bị hòa tan hết vì NaOH dư.
=> Chất rắn còn lại là Mg = 0,6 (g)
=> nMg = 0,6/24 = 0,025 mol
* TN1:
nH2 = 1,568/22,4 = 0,07mol
Gọi x là số mol Al.
PTHH: 2Al + 3H2SO4 -> Al2(SO4)3 + 3H2
_______x _________________________1,5x
PTHH: Mg + H2SO4 -> MgSO4 + H2
______0,025 _________________0,025
Ta có: 1,5x + 0,025 = 0,07 => x = nAl = 0,03mol
=> m = mMg + mAl = 0,6 + 0,03.27 = 1,41g
=> %Mg = (0,6/1,41).100% = 42,55%
=> %Al = 100% - 42,55% = 57,45%.

a) Gọi `n_{Al} = a (mol); n_{Fe} = b (mol)`
PTHH:
`2Al + 3H_2SO_4 -> Al_2(SO_4)_3 + 3H_2`
`Fe + H_2SO_4 -> FeSO_4 + H_`
b) `n_{H_2} = (0,56)/(22,4) = 0,025 (mol)`
Theo PT: `n_{H_2} = n_{Fe} + 3/2 n_{Al}`
`=> b + 1,5a = 0,025`
Giải hpt \(\left\{{}\begin{matrix}27a+56b=0,83\\1,5a+b=0,025\end{matrix}\right.\Leftrightarrow a=b=0,01\)
=> \(\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,01.27}{0,83}.100\%=32,53\%\\\%m_{Fe}=100\%-32,53\%=67,47\%\end{matrix}\right.\)

mdd giảm = m↓ - mCO2 → mCO2 = 10 - 3,4 = 6,6 gam → nCO2 = 6,6 : 44 = 0,15 mol.
C6H12O6 enzim−−−−→30−35oC→30-35oCenzim2C2H5OH + 2CO2
Theo phương trình: nC6H12O6 = 0,15 : 2 = 0,075 mol.
Mà H = 90% → nC6H12O6 = 0,075 : 90% = 1/12 mol → m = 180 x 1/12 = 15 gam

a) 2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
b) \(\left\{{}\begin{matrix}\%Fe=\dfrac{8}{15}.100\%=53,33\%\\\%Al=\dfrac{15-8}{15}.100\%=46,67\%\end{matrix}\right.\)





Ở thí nghiệm 2: Chỉ có Al tác dụng với dung dịch NaOH và bị hòa tan hết vì NaOH dư.
Chất rắn còn lại là Mg = 0,6 gam hay = 0,6 : 24 = 0,025 mol
Ở thí nghiệm 1: Số moi H2 = 1,568 : 22,4 = 0,07 mol. Gọi x là số mol Al.
Phương trình hóa học:
2Al + 3H2S04 \(\rightarrow\) Al2(S04)3 + 3H2
x \(\rightarrow\) 1,5x (mol)
Mg + H2S04 \(\rightarrow\) MgS04 + H2
0,025 \(\rightarrow\) 0,025 (mol)
Theo hiđro, ta có: 1,5x + 0,025 = 0,07 => x = 0,03 mol = mol Al Khối lượng của hỗn hợp: m = mMg + mAl = 0,6 + 0,03.27 = 1,41 gam
%Mg = \(\dfrac{0,6}{1,41}\) x 100% = 42,55%; %Al = 100% - 42,55% = 57,45%.
Ở thí nghiệm 2: Chỉ có Al tác dụng với dung dịch NaOH và bị hòa tan hết vì NaOH dư.
Chất rắn còn lại là Mg = 0,6 gam hay = 0,6 : 24 = 0,025 mol
Ở thí nghiệm 1: Số moi H2 = 1,568 : 22,4 = 0,07 mol. Gọi x là số mol Al.
Phương trình hóa học:
2Al + 3H2S04 → Al2(S04)3 + 3H2
x → 1,5x (mol)
Mg + H2S04 → MgS04 + H2
0,025 → 0,025 (mol)
Theo hiđro, ta có: 1,5x + 0,025 = 0,07 => x = 0,03 mol = mol Al Khối lượng của hỗn hợp: m = mMg + mAl = 0,6 + 0,03.27 = 1,41 gam
%Mg =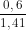 x 100% = 42,55%; %Al = 100% - 42,55% = 57,45%.
x 100% = 42,55%; %Al = 100% - 42,55% = 57,45%.