Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nHCl = 0,3.0,5 = 0,15 (mol) ; nCO2= 1,12 :22,4 = 0,05 (mol)
Khi nhỏ từ từ dd HCl vào dung dịch hỗn hợp NaHCO3 và Na2CO3 sẽ xảy ra phản ứng theo thứ tự:
HCl + Na2CO3 → NaHCO3 + NaCl (1)
HCl + NaHCO3 → CO2 + H2O (2)
Vì dung dịch X sau phản ứng + Ca(OH)2 dư thu được 20 gam kết tủa nữa => trong dd X có chứa NaHCO3 dư => HCl phản ứng hết
2NaHCO3 + Ca(OH)2 dư → CaCO3 + Na2CO3 + H2O (3)
0,4 ← 0,2 (mol)
nCaCO3 = 20 :100 = 0,2 (mol)
Từ PTHH (3) => nNaHCO3 dư = 2nCaCO3 = 0,4 (mol)
HCl+ Na2CO3 → NaHCO3 + NaCl (1)
(0,15 – 0,05) → 0,1 → 0,1 (mol)
HCl + NaHCO3 → CO2 + H2O (2)
0,05 ← 0,05 ← 0,05 (mol)
Từ PTHH (2): nHCl(2) = nNaHCO3(2) = nCO2 = 0,05 (mol)
=> nHCl(1) = ∑ nHCl – nHCl(2) = 0,15 – 0,05 = 0,1 (mol)
Từ PTHH (1): nNa2CO3 = nHCl = 0,1 (mol)
nNaHCO3(1) = nHCl(1) = 0,1 (mol)
Ta có: nNaHCO3(1) + nNaHCO3 bđ = nNaHCO3(2) + nNaHCO3 dư
=> nNaHCO3 bđ = 0,05 + 0,4 – 0,1 = 0,35 (mol)
=> a = mNa2CO3 + mNaHCO3 bđ = 0,1.106 + 0,35.84 = 40 (g)

\(n_{\downarrow}=\dfrac{35}{100}=0,35mol\Rightarrow n_C=m_{CaCO_3}=0,35mol\)
\(\left\{{}\begin{matrix}CH_4:x\left(mol\right)\\C_2H_2:y\left(mol\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x+y=\dfrac{4,48}{22,4}=0,2\\BTC:x+2y=0,35\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,05\\y=0,15\end{matrix}\right.\)
\(m_{tăng}=m_{Br_2}=2n_{C_2H_2}\cdot160=48g\)
\(\%V_{CH_4}=\dfrac{0,05}{0,05+0,15}\cdot100\%=25\%\)
\(\%V_{C_2H_2}=100\%-25\%=75\%\)
Gọi \(\left\{{}\begin{matrix}n_{CH_4}=x\\n_{C_2H_2}=y\end{matrix}\right.\)
\(n_{hh}=\dfrac{4,48}{22,4}=0,2mol\)
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
x x ( mol )
\(2C_2H_2+5O_2\rightarrow\left(t^o\right)4CO_2+2H_2O\)
y 2y ( mol )
\(n_{CaCO_3}=\dfrac{35}{100}=0,35mol\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
0,35 0,35 ( mol )
Ta có:
\(\left\{{}\begin{matrix}x+y=0,2\\x+2y=0,35\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,05\\y=0,15\end{matrix}\right.\)
\(m_{tăng}=2m_{C_2H_2}=2.0,15.160=48g\)
\(V_{CH_4}=0,05.22,4=1,12l\)
\(V_{C_2H_2}=0,15.22,4=3,36l\)

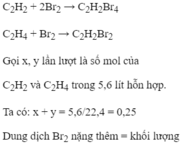
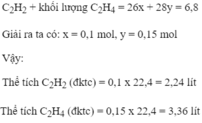


Đáp án B
Khí CO2 bị hấp thụ hết, khí thoát ra ngoài là khí C2H2 tinh khiết
PTHH : $CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O$
Đáp án B