Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Điều chế MgCl2 bằng:
- Phản ứng hóa hợp: Mg + Cl2 → MgCl2
- Phản ứng thế: Mg + CuCl2 → MgCl2 + Cu
- Phản ứng trao đổi: Mg(OH)2 + 2HCl → MgCl2 + 2H2O

$a\bigg)$
$Cl_2+H_2O\leftrightharpoons HCl+HClO$
$CH_4+Cl_2\xrightarrow{ánh\, sáng}CH_3Cl+HCl$
$CH_3Cl+Cl_2\xrightarrow{ánh\, sáng}CH_2Cl_2+HCl$
$CH_2Cl_2+Cl_2\xrightarrow{ánh\, sáng}CHCl_3+HCl$
$CHCl_3+Cl_2\xrightarrow{ánh\, sáng}CCl_4+HCl$
$b\bigg)$
- Chất khử:
$2KMnO_4+16HCl\to 2KCl+2MnCl_2+5Cl_2+8H_2O$
- Chất oxi hóa:
$Fe+2HCl\to FeCl_2+H_2$
- Chất trao đổi:
$AgNO_3+HCl\to AgCl\downarrow+NaNO_3$

a)
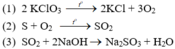
Phản ứng oxi hóa – khử là (1) và (2).
b)
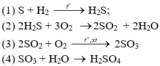
Phản ứng oxi hóa – khử là: (1), (2), (3)

\(a) 2Fe + 6H_2SO_4 \to Fe_2(SO_4)_3 + 3SO_2 + 6H_2O\)(Phản ứng oxi hóa-khử)
\(Fe_2O_3 + 3H_2SO_4 \to Fe_2(SO_4)_3 + 3H_2O\)
\(b) n_{SO_2} = \dfrac{672}{1000.22,4} = 0,03(mol)\\ n_{Fe}= \dfrac{2}{3}n_{SO_2} = 0,02(mol)\\ \%m_{Fe} = \dfrac{0,02.56}{2,72}.100\% = 41,18\%\\ \%m_{Fe_2O_3} = 100\% -41,18\% = 58,82\%\)

tham Khảo đi :
pp hóa hợp: Mg + Cl2 ---> MgCl2
pư thế: Mg + 2HCl ---> MgCl2 + H2
pư trao đổi: MgSO4 + BaCl2 ---> MgCl2 + BaSO4

a) Khí H2S và axit sunfuric đặc tham gia các phản ứng oxi hóa – khử thì khí H2S chỉ thể hiện tính khử và H2SO4 đặc chỉ thể hiện tính oxi hóa. Vì trong H2S số oxi hóa của S chỉ có thể tăng, trong H2SO4 số oxi hóa S chỉ có thể giảm.
Vì trong H2S số oxi hóa của S là -2 (là số oxi hóa thấp nhất của S) nên chỉ có thể tăng (chỉ thể hiện tính khử), trong H2SO4 số oxi hóa của S là +6 (là số oxi hóa cao nhất của S) nên chỉ có thể giảm (chỉ thể hiện tính oxi hóa).
b) Phương trình phản ứng hóa học:
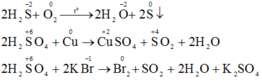

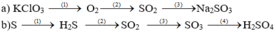

a, Pứ hóa hợp
\(\text{Mg + Cl2 ---> MgCl2}\)
Pứ oxh - khử. vì có sự thay đổi số oxhi hóa, Mg từ số oxh 0 lên +2; Clo từ 0 xuống -1
b, Pứ thế
\(\text{Mg +2 HCl ---> MgCl2 + H2}\)
--> Pứ oxh - khử.vì có sự thay đổi số oxhi hóa, Mg từ số oxh 0 lên +2, H từ +1 xuống 0
c, Pứ trao đổi
\(\text{MgSO4 + BaCl2 ---> MgCl2 + BaSO4 }\)
-> Ko là pứ oxh - k. vì k có sự thay đổi số oxh