Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Pha chế 50ml dung dịch H 2 S O 4 1,5M.
- Số mol H 2 S O 4 cần pha chế 50ml dung dịch H 2 S O 4 1,5M:
n H 2 S O 4 = CM.V = 1,5.0,05 = 0,075 (mol)
Gọi x(ml) là thể tích của dung dịch H 2 S O 4 1M (1)
Gọi y(ml) là thể tích của dung dịch H 2 S O 4 3M (2)
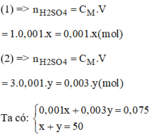
Giải hệ phương trình ta có: x = 37,5ml; y = 12,5ml
- Cách pha chế:
+ Đong lấy 37,5ml dung dịch H 2 S O 4 1M và 12,5ml dung dịch H 2 S O 4 3M cho vào bình, lắc đều, ta được 50ml dung dịch H 2 S O 4 1,5M.

Giải:
Số mol của dd HCl 10% là:
nHCl(1) = (C%.mdd)/(100.M) = (10.150.1,047)/(100.36,5) ≃ 0,43 (mol)
Số mol của dd HCl 2M là:
nHCl(2) = CM.V = 2.0,25 = 0,5 (mol)
Nồng độ mol của dd HCl thu được là:
CMHCl(3) = n/V = (0,43 + 0,5)/(0,15 + 0,25) = 2,325 (M)
Vậy ...
số mol của dd HCL 10% là:
nHCL=(C%.mdd)/(100.M)=(10.150.1.0,47)/(100.36,5)~0,43 (mol)
số mol của dd HCL 2M là:
nHCl=\(_{C_M}\).V=2.0,25=0,5(mol)
nồng đọ mol của dd HCL thu đc là:
\(C_m\)HCL=n/V=(0,43+0,5)/(0,15+0,25)=2,3(M)
vậy dung dịch mới thu được có nồng độ mol là 2,3M
1, dd HCl 37%, D=1,19g/ml. Nồng độ mol của dd là bn?
2, Nồng độ % của dd HCl 10,81M, D= 1,17g/ml là?

1.\(C_M=\dfrac{10.D.C\%}{M}=\dfrac{10.1,19.37}{36,5}\approx12,063M\)
2.\(C\%=\dfrac{C_M.M}{10.D}=\dfrac{10,81.36,5}{10.1,17}\approx33,724\%\)
Toshiro Kiyoshi nếu bạn cần phương pháp chứng minh thì đây nha bạn
C% = .100 (1)
mdd = V.D (2)
CM = 1000 (3)
Thế (2) và (3) vào (1) ta được:
C% = 100 => n =
(4)
Thế (4) vào (3) : CM =

bài 3:a) nCaCO3 = 0,07 mol
CaCO3 + 2HNO3 ---> Ca(NO3)2 + H2O + CO2
0.07.........0.14
=> nHNO3 trong Z là 0,14*2 = 0,28 mol
=> CM Z = 0,28/(0,3+0,2) = 0,56 M
gọi CM dd Y = b M; CM dd X = a M
nHNO3 trong X = 0,2*a mol
=> nHNO3 trong Y = 0,3*b mol
X điều chế từ Y nghĩa là từ dd Y ta có thể điều chế một dd có nồng độ mol/lit giống Y
=> đặt V dd Y đạ dùng để điều chế X là V (lit)
=> CM X' = nHNO3/(V H2O + V dd Y)
hay = b* V/(V+3V) = a
=> 4a = b
mà theo câu a ta lại có :
n HNO3 trong X + nHNO3 trong Y = 0,2*a + 0,3*b = 0,28
giải hệ ta đk; x = 0,2M
y = 0,8M

số mol của dd HCL 10% là:
nHCL=(C%.mdd)/(100.M)=(10.150.1.0,47)/(100.36,5)~0,43 (mol)
số mol của dd HCL 2M là:
nHCl=CMCM.V=2.0,25=0,5(mol)
nồng đọ mol của dd HCL thu đc là:
CmCmHCL=n/V=(0,43+0,5)/(0,15+0,25)=2,3(M)
vậy dung dịch mới thu được có nồng độ mol là 2,3M

Câu 1 :
Trong 150 ml dung dịch HCl 10% có D = 1,047 g/ml có:
m dd HCl = D.V = 150.1,047 = 157,05(gam)
n HCl = 157,05.10%/36,5 = 0,43(mol)
Trong 250 ml dung dịch HCl 2M có :
n HCl = 0,25.2 = 0,5(mol)
Sau khi trộn :
n HCl = 0,43 + 0,5 = 0,93(mol)
V dd = 150 + 250 = 400(ml) = 0,4(lít)
Suy ra :CM HCl = 0,93/0,4 = 2,325M
Đáp án C

\(m_{ddHCl.20\%}=2000\times1,1=2200\left(g\right)\)
\(\Rightarrow m_{HCl.20\%}=2200\times20\%=440\left(g\right)\)
Gọi x,y lần lượt là khối lượng dd của dd HCl.36% và dd HCl.12%
\(\Rightarrow m_{HCl.36\%}=x\times36\%=\frac{9}{25}x\left(g\right)\)
\(m_{HCl.12\%}=y\times12\%=\frac{3}{25}y\left(g\right)\)
Ta có: \(\left\{{}\begin{matrix}x+y=2200\\\frac{9}{25}x+\frac{3}{25}y=440\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=733,33\\y=1466,67\end{matrix}\right.\)
Vậy \(m_{ddHCl.36\%}=733,33\left(g\right)\)
\(m_{ddHCl.12\%}=1466,67\left(g\right)\)


Gọi số ml dd HCl ở lọ 1 và 2 lần lượt là:a;b(ml)
V của dd HCl 1M là:a
V của dd HCl 3M là:3b
Ta có:
CM=\(\dfrac{a+3b}{a+b}=2\)(a+b=50)
\(\Leftrightarrow a+3b=100\)
\(\Leftrightarrow2b=50\)
\(\Leftrightarrow b=25\)
\(\Rightarrow a=25\)
Vậy để pha chế 50 ml dd HCl 2M thì ta cần đổ 25ml dd HCl 1M và 25ml dd HCl 3M
Gọi a, b lần lượt là thể tích dung dịch HCl của lọ thứ 1và lọ thứ 2 (a, b > 0 , lít)
=>: \(a+b=0,05\left(I\right)\)
Ta có: \(n_{HCl}\)(lọ 1) \(=a.1=a\left(mol\right)\)
\(n_{HCl}\)(lọ 2) \(=3b\left(mol\right)\)
\(n_{HCl}\left(sau\right)=2.0,05=0,1\left(mol\right)\)
\(\Rightarrow a+3b=0,1\left(II\right)\)
Từ (I) và (II) \(\Rightarrow\left\{{}\begin{matrix}a=0,025\left(lit\right)=25\left(ml\right)\\b=0,025\left(lit\right)=25\left(ml\right)\end{matrix}\right.\)
Vậy....