Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)
$CO + CuO \xrightarrow{t^o} Cu + CO_2$
$CO_2 + 2NaOH \to Na_2CO_3 + H_2O$
$Na_2CO_3 + BaCl_2 \to BaCO_3 + 2NaCl$
b)
n CO2 = n BaCO3 = n/197 (mol)
Nếu V/22,4 > m / 80 thì H =( m/80 : n/197) .100% = 197m/80n .100%
Nếu V/22,4 < m / 80 thì H =( V/22,4 : n/197) .100% = 197V/22,4m .100%
c)
Nếu thay CO bằng khí H2 thì kết quả thay đổi hoàn toàn ra khí sinh ra hấp thụ vào NaOH không tạo kết tủa với BaCl2

số mol của BaCO3 là nBaCO3 =39,4/197=0,2 (mol)
mH2SO4= 98*60/100=58,8 (g)
nH2SO4 = 58,8/98 = 0,6 (mol)
PTPỨ
CuO + CO ----------> Cu +CO2
CO2 + Ba(OH)2 ------------> BaCO3 + H2O
0,2 0,2 mol
Cu + 2H2SO4 -------------> CuSO4 + SO2 + 2H2O
0,3 0,6 mol
còn lại khối lượng và thành phần phần trăm bạn tự tính nha

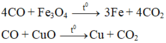
![]()
Khí thoát ra khỏi bình dẫn qua dung dịch Ca OH 2 thu được 5 gam kết tủa CaCO 3
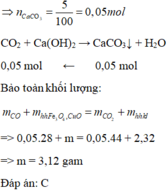

C + 2H2O CO2 + 2H2
C + CO2 2CO
Khí X gồm 3 khí : CO2, H2, CO.
Dẫn ½ lượng X qua dd Ba(OH)2 chỉ có CO2 tham gia phản ứng. Phản ứng thu được kết tủa nên có thể xảy ra các PTHH sau:
CO2 + Ba(OH)2→ BaCO3↓ + H2O
2CO2 + Ba(OH)2 → Ba(HCO3)2
Dẫn ½ lượng khí X trên ( lấy dư so với lượng cần thiết) qua hỗn hợp CuO và Na2O có thể xảy ra các PTHH là:
H2 + CuO → t ∘ Cu + H2O
CO + CuO → t ∘ Cu + CO2
CO2 + Na2O → Na2CO3
H2O + Na2O → 2NaOH
CO2 + 2NaOH → Na2CO3 + H2O
CO2 + NaOH → NaHCO3
Chú ý:
sản phẩm H2O sinh ra có phản ứng với Na2O

\(1.\)\(Fe_2O_3+3CO\underrightarrow{^{^{t^0}}}3Fe+3CO_2\)
\(2.\)\(Fe_2O_3+3CO\underrightarrow{^{^{t^0}}}3Fe+3CO_2\)
\(3.Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
\(4.Ca\left(OH\right)_2+2CO_2\rightarrow Ca\left(HCO_3\right)_2\)
\(5.Ba\left(OH\right)_2+CO_2\rightarrow BaCO_3+H_2O\)
1) \(Fe_2O_3+3CO\underrightarrow{t^o}2Fe+3CO_2\)
2)
\(Fe_2O_3+3CO\underrightarrow{t^o}2Fe+3CO_2\)
3) \(Ca\left(OH\right)_2+CO_2->CaCO_3\downarrow+H_2O\)
4) \(Ca\left(OH\right)_2+CO_2->CaCO_3\downarrow+H_2O\)
\(CaCO_3+CO_2+H_2O->Ca\left(HCO_3\right)_2\)
5) \(Ba\left(OH\right)_2+CO_2->BaCO_3\downarrow+H_2O\)


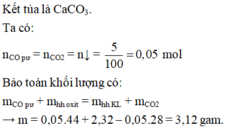

\(a.CO+CuO\xrightarrow[]{t^0}Cu+CO_2\\ CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\\ n_{CaCO_3}=\dfrac{16}{100}=0,16mol\\ n_{CuO}=n_{CO_2}=n_{CaCO_3}=0,16mol\\ \%m_{CuO,pư}=\dfrac{0,16.80}{20}\cdot100=64\%\)