Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B.
Áp dụng định luật bảo toàn khối lượng:
![]()
= 30,1 - 11,1 = 19 gam
Đặt
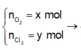
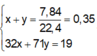
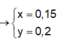
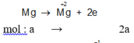
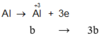
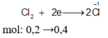
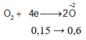
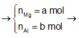
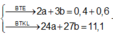
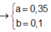
![]()

Đáp án C
nMg=nFe=9,6/(24+56)=0,12 mol
nO=nH+/2=0,36/2=0,18 mol => nO2=0,09 mol
nCl2=z
Giả sử trong Y:
Fe2+: x
Fe3+: y
Cl-: 2z+0,36 (BTNT Cl)
Fe2+ + Ag+ → Fe3+ + Ag
x x
Ag+ + Cl- → AgCl
2z+0,36 2z+0,36
BTNT Fe: x+y=0,12 (1)
BT e: 0,12.2+2x+3y=2z+0,18.2 (2)
m kết tủa = 108x+143,5(2z+0,36) = 85,035 (3)
Giải hệ pt ta được: x=0,03; y=0,09; z=0,105
%VO2=0,09/(0,09+0,105)=46,15%

Đáp án A
► Đặt nCl2 = a; nO2 = b ⇒ nY = a + b = 0,45 mol.
Bảo toàn electron: 2a + 4b = 0,3 × 2 + 0,2 × 3 ||⇒ giải hệ cho:
a = 0,3 mol; b = 0,15 mol ⇒ %mO2 = 18,39%.
● Bảo toàn khối lượng: x = 51(g)

Đáp án A
► Đặt nCl2 = a; nO2 = b
⇒ nY = a + b = 0,45 mol.
Bảo toàn electron: 2a + 4b = 0,3 × 2 + 0,2 × 3
⇒ giải hệ cho:
a = 0,3 mol; b = 0,15 mol
⇒ %mO2 = 18,39%.
● Bảo toàn khối lượng: x = 51(g)

Giải thích: Đáp án B
Gọi số mol Cl2 và O2 lần lượt là x và y mol
=> ∑ nhh = x + y = 0,45 (mol)
∑ n e (KL nhường) = ∑ n e ( Cl2, O2 nhận) <=> 2.0,3 + 3.0,2 = 2x + 4y (2)
Từ (1) và ( 2) => x = 0,3 và y = 0,15 mol
% mO2 = [ ( 0,15.32): ( 0,15.32 + 0,3.71)]. 100% = 18,39%
BTKL: x = mKL + mhh khí = 0,3.65 + 0,2.27 + 0,3.71 + 0,15. 32 = 51 (g)

Đáp án D:
Gọi x, y lần lượt là số mol của Cl2 và O2 có trong 0,2 mol hỗn hợp khí Y =>x+y = 0,2(1)
Theo định luật bảo toàn khối lượng:
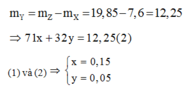
Gọi a, b lần lượt là số mol của Mg và Ca
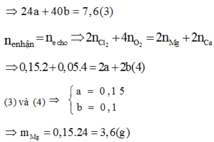


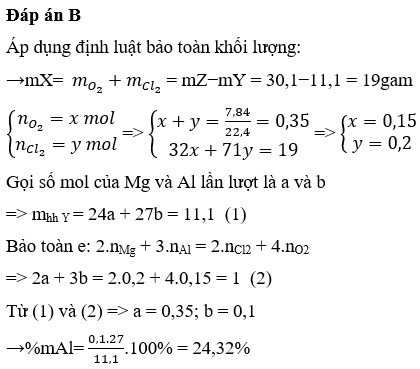
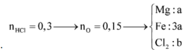
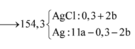
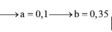

Đáp án B.
Định hướng tư duy giải