Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Chất phân ly ra nồng độ OH- càng cao thì pH càng lớn.

Chọn đáp án A.
H2SO4 là một axit mạnh, CH3COOH là axit yếu.
KNO3 có môi trường trung tính.
Na2CO3 có môi trường bazơ

Chọn đáp án D
Chất nào có tình axit càng mạnh thì PH càng nhỏ,ngược lại chất nào có tính bazo càng mạnh thì PH càng lớn.

Đáp án C
pH = - log[H+]
Nồng độ H+ càng cao thì pH càng nhỏ => pH (H2SO4) < pH (HCl)
Na2CO3 là muối của bazo mạnh và axit yếu => môi trường bazo
KNO3 là muối của kiềm mạnh và axit mạnh => môi trường trung tính

Sau phản ứng, \(V_{dd}= V_1 + V_2(lít)\)
Ta có : [H+] = 10-3 ⇒ \(n_{H_2SO_4} = 5.10^{-4}V_1(mol)\)
Lại có: \(n_{NaOH} = V_2.\dfrac{10^{-14}}{10^{-12}} = 0,01V_2(mol)\)
pH = 4 < 7 Chứng tỏ axit dư
2NaOH + H2SO4 → Na2SO4 + 2H2O
0,01V2.......5.10-3V2..................................(mol)
Suy ra : \(\dfrac{5.10^{-4}V_1-5.10^{-3}V_2}{V_1+V_2}.2 = 10^{-4}\\ \Rightarrow \dfrac{V_1}{V_2} = \dfrac{101}{9}\)
Đáp án B

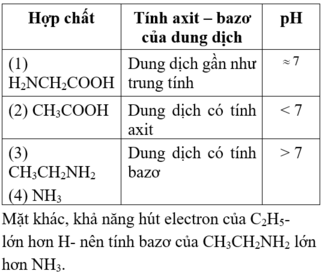


Chọn B
Thứ tự giảm dần pH:
Ba ( OH ) 2 (pH = 12,3) > NaOH (pH = 12) > Na 2 SO 4 (pH = 7) > H 2 SO 4 (pH = 1,7).