Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 3. Trong dãy đơn chất từ F2 đến I2, chất có tính oxi hóa mạnh nhất là
A. F2
B. Cl2
C. Br2
D. I2

Câu 1: Các nguyên tố nhóm VIIA có cấu hình electron lớp ngoài cùng dạng tổng quát là
A. 3s23p5 B. 2s22p5 C. 4s24p5 D. ns2np5
Câu 2: Halogen nào sau đây ở nhiệt độ thường là chất khí màu lục nhạt, rất độc?
A.Clo. B. Brom. C. Flo. D. Iot.
Câu 3: Tính chất vật lý đặc biệt của iot là
A. tan nhiều trong nước B. Dễ chảy rữa C. dễ thăng hoa D. Màu nâu đỏ
Câu 4: Phi kim nào sau đây là chất lỏng màu đỏ nâu, dễ bay hơi, rất độc?
A.Clo. B. oxi. C. Brom. D. Hidro.
Câu 5: Liên kết trong phân tử của các đơn chất halogen là
A. liên kết cộng hoá trị có cực. B. liên kết cộng hóa trị không có cực.
C. liên kết kim loại D. liên kết ion.
Câu 6: Tính chất hóa học đặc trưng của nhóm halogen là
A. tính khử B. Không có tính khử và không có tính oxi hóa.
C. Tính oxi hóa D. vừa có tính khử, vừa có tính oxi hóa
Câu 7:Dãy các nguyên tố halogen có tính oxi hóa tăng dần là
A. Cl, F, Br, I B. Cl, Br, I, F C. I, Br, Cl, F D. Br, I, F, ClCâu
Câu 11: Cho từng chất KMnO4, MnO2, KClO3, K2Cr2O7 có cùng số mol tác dụng hoàn toàn với dung dịch HCl đặc, dư thì chất cho lượng khí Cl2 ít nhất là:
A. KMnO4 B. MnO2 C. KClO3 D. K2Cr2O7
Câu 12: Trong phòng thí nghiệm, Clo thường được điều chế theo phản ứng
HClđặc + KMnO4 → KCl + MnCl2 + Cl2 + H2O
Hệ số cân bằng của phương trình trên lần lượt là
A. 16; 2; 2; 2; 5; 8 B. 8; 2; 5; 2; 2; 4 C. 2; 16; 2;2; 5; 8 D. 16; 5; 2; 2; 8; 2
Câu 13: Trong phòng thí nghiệm, Clo thường được điều chế theo phản ứng
HClđặc + MnO2 → MnCl2 + Cl2 + H2O
Hệ số cân bằng của phương trình trên lần lượt là
A. 4; 1; 1;1; 2 B. 4; 2; 2; 2; 1 C. 2; 4; 2;2; 1 D. 1; 4; 1; 1; 2
Câu 14: Thành phần chính của nước javen là:
A. NaCl và NaClO. B. NaCl và HclO C. NaClO. D. NaCl.
Câu 15: Hiện tượng xảy ra khi nhỏ dung dịch AgNO3 vào dung dịch NaI
A. Xuất hiện kết tủa màu trắng B. Xuất hiện kết tủa màu vàng nhạt
C. Xuất hiện kết tủa màu vàng đậm D. Không có hiện tượng gì
Câu 16: Chất nào sau đây không tác dụng với dd HCl?
A. Fe. B. Cu. C. AgNO3. D. CaCO3
1D, 2A, 3C, 4C, 5B, 6C, 7C, 8C, 9B, 10A, 11D, 12A, 13A, 14A, 15C, 16B

1)
a. Vì R có công thức oxit cao nhất là \(RO_3\) nên nên trong hợp chất với hidro, hợp chất của R sẽ có dạng: \(H_2R\).
Theo đề, trong \(H_2R\) có 94,12% \(R\) về khối lượng:
\(\Leftrightarrow\dfrac{R}{2+R}.100=94,12\Leftrightarrow R=32\)
Vậy R là \(S\) (lưu huỳnh); công thức oxit cao nhật của lưu huỳnh là \(SO_3\).
b. Có: \(n_{SO_3}=\dfrac{8}{80}=0,1\left(mol\right);n_{NaOH}=0,15.0,1=0,015\left(mol\right)\)
Có tỉ lệ: \(\dfrac{n_{SO_3}}{n_{NaOH}}=\dfrac{0,015}{0,1}=0,15< 1\)
\(\Rightarrow\) Muối sau phản ứng là NaHSO3.
PTHH: \(SO_3+NaOH\rightarrow NaHSO_3\)
0,015(mol) --> 0,015(mol)
Vì \(n_{SO_3}>n_{NaOH}\) nên \(SO_3\) dư.
Theo phương trình, \(n_{NaHSO_3}=n_{NaOH}=0,015\left(mol\right)\)
\(\Rightarrow m_{NaHSO_3}=0,015.104=1,56\left(g\right)\)
2)
a. Vì R có cấu hình electron lớp ngoài cùng là \(ns^2np^3\) nên trong hợp chất với oxi, công thức oxit cao nhất của R có dạng: \(R_2O_5\).
Theo đề, trong \(R_2O_5\), Oxi chiếm 56,34% về khối lượng.
\(\Leftrightarrow\dfrac{16.5}{2R+16.5}.100=56,34\Leftrightarrow R=31\)
Vậy R là P - Photpho.
b. Theo đề: \(n_{P_2O_5}=\dfrac{14,2}{142}=0,1\left(mol\right)\)
PTHH: \(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
0,1(mol) ------------> 0,2(mol)
Theo phương trình \(\rightarrow n_{H_3PO_4}=2n_{P_2O_5}=0,2\left(mol\right)\)
\(\Rightarrow m_{H_3PO_4}=0,2.98=19,6\left(g\right)\)
Mặt khác: mdung dịch thu được = \(m_{P_2O_5}+m_{H_2O}\)
= \(14,2+100=114,2\left(g\right)\)
\(\Rightarrow C\%_{H_3PO_4}=\dfrac{m_{H_3PO_4}}{m_{dd}}.100=\dfrac{19,6}{114,2}.100=17,163\%\)

a) CT hợp chất khí cao nhất : RH3
=> CT hợp chất với O : R2O5
%R = 2R/(2R + 16*5) *100% = 43.66%
<=> R = 31
=> R : P
b)
R thuộc nhóm VII A => R có hóa trị cao nhất với O là VII
=> CT hợp chất khí với H : RH
%H = 1/(R+1) *100% = 39/50%
=> R = 127
=> R là : I
c) R thuộc nhóm VII A => R có hóa trị cao nhất với O là: VII
=> CT : R2O7
%R = 2R/(2R + 16*7) *100% = 38.79%
=> R = 35.5
=> R là : Cl
d) Oxit cao nhất là : R2O5
=> CT hợp chất khí với H : RH3
%H = 3/(R+3) *100% = 17.65%
=> R = 14
=> R là : N
a)
công thức hợp chất của R với H là RH3 => công thức oxit cao nhất của R là R2O5
ta có : 2R / 2R + 16.5 = 43,66%
=> R= 31 => photpho
c) CTHH:R2O7
R chiếm 38.79%
Suy ra
\(\frac{2R}{2R+16.7}=\)0,3879
=>2R=0,,7758R+42,44
=>1,22R=43,44
=>R=36 Xem lại đề
d)
R2O5
công thức với hidro là : RH3
Ta có : R/R+3=0,9118⇒R=31 là P
f) R+2HCl--->RCl2+H2
n\(_{H2}=\frac{4,48}{22,4}=0,2\left(mol\right)\)
Theo pthh
n\(_R=n_{H2}=0,2\left(mol\right)\)
M\(_M=\frac{13}{0,2}=65\left(Zn\right)\)

A: H2
B: HCl
C: FeCl2
D: FeCl3
E: NaOH
F: Fe(OH)3
G: Fe2O3
H: H2O
PTHH:
(1): Cl2 + H2 =(nhiệt)=> 2HCl
(2): 2HCl + Fe ===> FeCl2 + H2
(3): 2FeCl2 + Cl2 ===> 2FeCl3
(4): FeCl3 + 2NaOH ===> Fe(OH)3\(\downarrow\) + 2NaCl
(5): 2Fe(OH)3 =(nhiệt)=> Fe2O3 + 3H2O
(6): Fe2O3 + 3H2 =(nhiệt)=> 2Fe + 3H2O

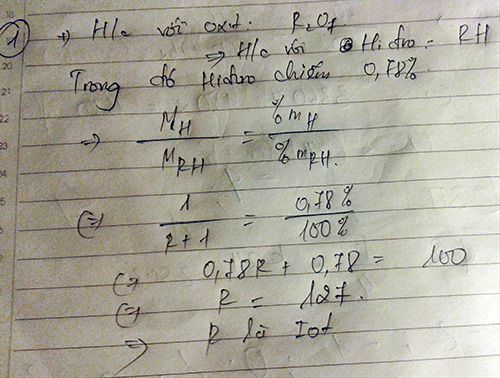

Chọn đáp án D
Từ F 2 đến I 2 nhiệt độ sôi tăng dần → I 2 có nhiệt độ sôi cao nhất.