Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nNa2CO3=0,3.0,5=0,15(mol)
nBaCl2=0,2.0,1=0,02(mol)
nBa(NO3)2=0,2.0,2=0,04(mol)
Đặt CT chung của muối Ba là BaX2
nBaX2=0,02+0,04=0,06(mol)
PT Na2CO3 + BaX2 -->BaCO3 + 2NaX
->nBaCO3=nNa2CO3=0,15(mol)
->mBaCO3=0,15.197=29,55(g)
Ta có: \(n_{CO_3^{2-}}=n_{Na_2CO_3}=03.0,5=0,15\left(mol\right)\)
\(n_{Ba^{2+}}=n_{BaCl_2}+n_{Ba\left(NO_3\right)_2}=0,2.0,1+0,2.0,2=0,06\left(mol\right)\)
PT ion: \(CO_3^{2-}+Ba^{2+}\rightarrow BaCO_{3\downarrow}\)
______0,15____0,06__→ 0,06 (mol)
\(\Rightarrow m_{\downarrow}=m_{BaCO_3}=0,06.197=11,82\left(g\right)\)
Bạn tham khảo nhé!

`100mL=0,1L`
`n_{H^+}=0,1.0,05.2+0,1.0,1=0,02(mol)`
`n_{SO_4^{2-}}=0,1.0,05=0,005(mol)`
`n_{OH^-}=0,1.0,2+0,1.0,1.2=0,04(mol)`
`n_{Ba^{2+}}=0,1.0,1=0,01(mol)`
`Ba^{2+}+SO_4^{2-}->BaSO_4`
Do `0,01>0,005->` Tính theo `SO_4^{2-}`
`n_{BaSO_4}=n_{SO_4^{2-}}=0,005(mol)`
`->m_↓=0,005.233=1,165(g)`
`H^{+}+OH^{-}->H_2O`
Do `0,02<0,04->OH^-` dư
`n_{OH^{-}\ pu}=n_{H^+}=0,02(mol)`
`->n_{OH^{-}\ du}=0,04-0,02=0,02(mol)`
Trong X: `[OH^-]={0,02}/{0,1+0,1}=0,1M`
`->pH=14-pOH=14+lg[OH^-]=13`

Chọn D
Bảo toàn điện tích có: 0,07 + 3a = 0,12 + 0,02.2 → a = 0,03 mol
Cho X vào hỗn hợp KOH và Ba(OH)2:
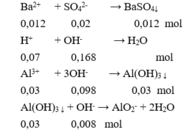
Sau phản ứng thu được kết tủa là:
BaSO 4 0,012 (mol) và Al ( OH ) 3 : 0,03 – 0,008 = 0,022 (mol).
m↓ = 0,012.233 + 0,022.78 = 4,512 gam.

a, \(n_{HCl}=0,2.0,1=0,02\left(mol\right)=n_{H^+}=n_{Cl^-}\)
\(n_{H_2SO_4}=0,2.0,15=0,03\left(mol\right)=n_{SO_4^{2-}}\) \(\Rightarrow n_{H^+}=2n_{H_2SO_4}=0,06\left(mol\right)\)
\(\Rightarrow\Sigma n_{H^+}=0,02+0,06=0,08\left(mol\right)\)
\(n_{Ba\left(OH\right)_2}=0,3.0,05=0,015\left(mol\right)=n_{Ba^{2+}}\)
\(\Rightarrow n_{OH^-}=2n_{Ba\left(OH\right)_2}=0,03\left(mol\right)\)
\(H^++OH^-\rightarrow H_2O\)
0,03___0,03 (mol) ⇒ nH+ dư = 0,05 (mol)
\(Ba^{2+}+SO_4^{2-}\rightarrow BaSO_4\)
0,015___0,015______0,015 (mol) ⇒ nSO42- dư = 0,015 (mol)
⇒ m = mBaSO4 = 0,015.233 = 3,495 (g)
\(\left[Cl^-\right]=\dfrac{0,02}{0,2+0,3}=0,04\left(M\right)\)
\(\left[H^+\right]=\dfrac{0,05}{0,2+0,3}=0,1\left(M\right)\)
\(\left[SO_4^{2-}\right]=\dfrac{0,015}{0,2+0,3}=0,03\left(M\right)\)
b, pH = -log[H+] = 1

\(n_{Ba^{2+}}=0,4.0,05=0,02mol\\ n_{OH^-}=0,04mol\\ m=98.0,02+233.0,02=6,62g\)

