Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{H_2}=\dfrac{1}{22,4}=\dfrac{5}{112}\left(mol\right)\)
\(n_{Cl_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
PTHH: H2 + Cl2 --as--> 2HCl
Xét tỉ lệ: \(\dfrac{\dfrac{5}{112}}{1}>\dfrac{0,03}{1}\) => Hiệu suất tính theo Cl2
\(n_{AgCl}=\dfrac{7,175}{143,5}=0,05\left(mol\right)\)
Bảo toàn Cl: \(n_{Cl_2\left(pư\right)}=0,025\left(mol\right)\)
\(H\%=\dfrac{0,025}{0,03}.100\%=83,33\%\)

\(n_{AgCl}=\dfrac{7,175}{143,5}=0,05\left(mol\right)\)
PTHH: HCl + AgNO3 ---> AgCl↓ + HNO3
0,05<---------------0,05
\(\rightarrow m_{HCl}=0,05.36,5=1,825\left(g\right)\\
\rightarrow C\%_{ddA}=\dfrac{1,825}{50}.100\%=3,65\%\)
\(n_{Cl_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Đặt H = x%
PTHH: Cl2 + H2 --as--> 2HCl
LTL: 6,72 < 10 => H2 dư
=> nHCl = 0,3x (mol)
\(\rightarrow C\%_{HCl}=\dfrac{0,3x.36,5}{0,3x.36,5+385,4}.100\%=3,65\%\\ \Leftrightarrow20,23\%\)

Ta có: \(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
\(n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right)\)
Theo ĐLBT e, có: 3nFe + 2nMg = nNO2 ⇒ nNO2 = 0,5 (mol)
BTNT Fe, có: nFe(NO3)3 = nFe = 0,1 (mol)
BTNT Mg, có: nMg(NO3)2 = nMg = 0,1 (mol)
BTNT N, có: nHNO3 = 3nFe(NO3)3 + 2nMg(NO3)2 + nNO2 = 1 (mol)

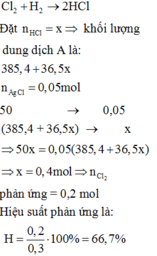





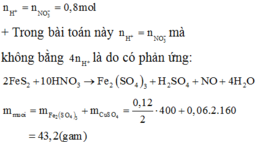


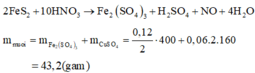

\(H_2 + Cl_2 \xrightarrow{ánh\ sáng} 2HCl\\ n_{H_2} < n_{Cl_2} \Rightarrow \text{Hiệu suất tính theo số mol }\ H_2\\ n_{H_2\ pư} = 0,3.80\% = 0,24(mol)\\ HCl + NaOH \to NaCl + H_2O\\ n_{NaOH} = n_{HCl} = 2n_{H_2\ pư} = 0,48(mol)\\ V_{dd\ NaOH} = \dfrac{0,48}{1} = 0,48(lít) = 480(ml) \)