Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Theo gt ta có: $n_{H_2}=0,75(mol)$
a, $2H_2+O_2\rightarrow 2H_2O$
Ta có: $n_{O_2}=0,5.n_{H_2}=0,375(mol)\Rightarrow V_{O_2}=8,4(l)\Rightarrow V_{kk}=42(l)$
b, $2KMnO_4\rightarrow K_2MnO_4+MnO_2+O_2$
Ta có: $n_{KMnO_4}=2.n_{O_2}=0,75(mol)\Rightarrow m_{KMnO_4}=118,5(g)$
a)
\(2H_2 + O_2 \xrightarrow{t^o} 2H_2O\\ V_{O_2} = \dfrac{V_{H_2}}{2} = \dfrac{16,8}{2} = 8,4(lít)\\ V_{không\ khí} = \dfrac{8,4}{20\%} = 42(lít)\)
b)
\(n_{O_2} = \dfrac{8,4}{22,4} = 0,375(mol)\\ 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\\ n_{KMnO_4} = 2n_{O_2} = 0,75(mol)\\ \Rightarrow m_{KMnO_4} = 0,75.158 = 118,5(gam)\\ 2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2\\ n_{KClO_3} = \dfrac{2}{3}n_{O_2} = 0,25(mol)\\ \Rightarrow m_{KClO_3} = 0,25.122,5 = 30,625(gam)\)

a.b.
\(n_{Fe}=\dfrac{16,8}{56}=0,3mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,3 0,2 0,1 ( mol )
\(m_{Fe_3O_4}=0,1.232=23,2g\)
\(V_{O_2}=0,2.22,4=4,48l\)
\(V_{kk}=4,48.5=22,4l\)
c.
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,4 0,2 ( mol )
\(m_{KMnO_4}=\dfrac{0,4.158}{\left(100-20\right)\%}=79g\)
a/ Số mol Fe là : nFe = 16,8: 56 = 0,3 mol
PTPƯ:
3Fe + 2O2 Fe3O4 (1)
Fe3O4 (1)
0,3 mol → 0,2mol → 0,1 mol
Từ (1) ta có số mol Fe3O4 = 0,1mol
→ m Fe3O4 = n.M = 0,1.232 = 23,2gam
b/ Từ (1) ta có số mol O2 đã dùng nO2 = 0,2 mol
Thể tích khí oxi đã dùng ở đktc: VO2 = n.22,4 = 0,2.22,4 = 4,48 lít
Thể tích không khí đã dùng: Vkk = 5. VO2= 5.4,48 = 22,4 lít.
c/ PTPƯ
2 KMnO4 K2MnO4 + MnO2 + O2 (2)
K2MnO4 + MnO2 + O2 (2)
0,4444mol ← 0,222mol
Vì lượng Oxi thu được hao hụt 10% nên số mol O2 cần có là:
nO2 = 0,2mol.100/90 = 0.222 mol
Từ (2) ta có số mol KMnO4 = 0,444mol
Khối lượng KMnO4 bị nhiệt phân
mKMnO4 = n.M = 0,444.158 = 70.152 gam

\(n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right)\\ a,2Mg+O_2\rightarrow\left(t^o\right)2MgO\\ n_{O_2}=\dfrac{0,1}{2}=0,05\left(mol\right)\\ V_{O_2\left(đktc\right)}=0,05.22,4=1,12\left(l\right)\\ b,2KClO_3\rightarrow\left(t^o\right)2KCl+3O_2\\ n_{KClO_3}=\dfrac{0,05.2}{3}=\dfrac{1}{30}\left(mol\right)\\ \Rightarrow m_{KClO_3}=\dfrac{122,5}{30}=\dfrac{49}{12}\left(g\right)\)

a) nFe = 16,8/56 = 0,3 (mol)
PTHH: 3Fe + 2O2 -> (t°) Fe3O4
Mol: 0,3 ---> 0,2 ---> 0,1
mFe3O4 = 0,1 . 232 = 23,2 (g)
b) VO2 = 0,2 . 22,4 = 4,48 (l)
Vkk = 4,48 . 5 = 22,4 (l)
c) H = 100% - 20% = 80%
nO2 (LT) = 0,2 : 80% = 0,25 (mol)
PTHH: 2KMnO4 -> (t°) K2MnO4 + MnO2 + O2
nKMnO4 = 0,25 . 2 = 0,5 (mol)
mKMnO4 = 0,5 . 158 = 79 (g)

a) \(n_P=\dfrac{6,2}{31}=0,2\left(mol\right)\)
PTHH: 4P + 5O2 --to--> 2P2O5
0,2-->0,25
=> VO2 = 0,25.22,4 = 5,6 (l)
=> Vkk = 5,6.5 = 28 (l)
b)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
0,5<-----------------------------0,25
=> \(m_{KMnO_4}=0,5.158=79\left(g\right)\)

nAl = 10,8: 27=0,4 (mol)
pthh : 4Al + 3O2 -t--->2 Al2O3
0,4---> 0,3 (mol)
=>VO2 = 0,3 .22,4 = 6,72 (l)
ta có : VO2 = 1/5 Vkk <=> Vkk = VO2 : 1/5= 33,6 (l)
pthh : 2KClO3 -t--> 2KCl + 3O2
0,2<---------------------0,3 (mol)
=> mKClO3 = 0,2 . 122,5 (g)
pthh : 2KMnO4-t--> K2MnO4 + MnO2+ O2
0,6<-------------------------------- 0,3(mol)
=> mKMnO4 = 0,6.158 = 94,8 (g)

a) PTHH: 4P+5O2-----to---> 2P2O5
0,2 0,25 0,1
b)\(n_{P_2O_5}=\dfrac{m}{M}=\dfrac{14,2}{142}=0,1\left(mol\right)\)
\(m_P=n.M=0,2.31=6,2\left(gam\right)\)
c) \(V_{O_2}=n.22,4=0,25.22,4=5,6\left(l\right)\)

4P (0,2 mol) + 5O2 (0,25 mol) \(\underrightarrow{t^o}\) 2P2O5.
a) Thể tích không khí cần dùng ở đktc là 0,25.22,4.5=28 (lít).
b) 2KMnO4 (0,5 mol) \(\underrightarrow{t^o}\) K2MnO4 + MnO2 + O2 (0,25 mol).
Khối lượng cần tìm là 0,5.158=79 (g).
a.\(n_P=\dfrac{6,2}{31}=0,2mol\)
\(4P+5O_2\rightarrow\left(t^o\right)2P_2O_5\)
0,2 0,25 ( mol )
\(V_{kk}=V_{O_2}.5=\left(0,25.22,4\right).5=28l\)
b.\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,5 0,25 ( mol )
\(m_{KMnO_4}=0,5.158=79g\)

a)\(n_{Fe}=\dfrac{22,4}{56}=0,4mol\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
0,4 \(\dfrac{4}{15}\) \(\dfrac{2}{15}\)
\(V_{O_2}=\dfrac{4}{15}\cdot22,4=5,973l\)
b)\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
\(\dfrac{8}{45}\) \(\dfrac{4}{15}\)
\(m_{KClO_3}=\dfrac{8}{45}\cdot122,5=21,78g\)

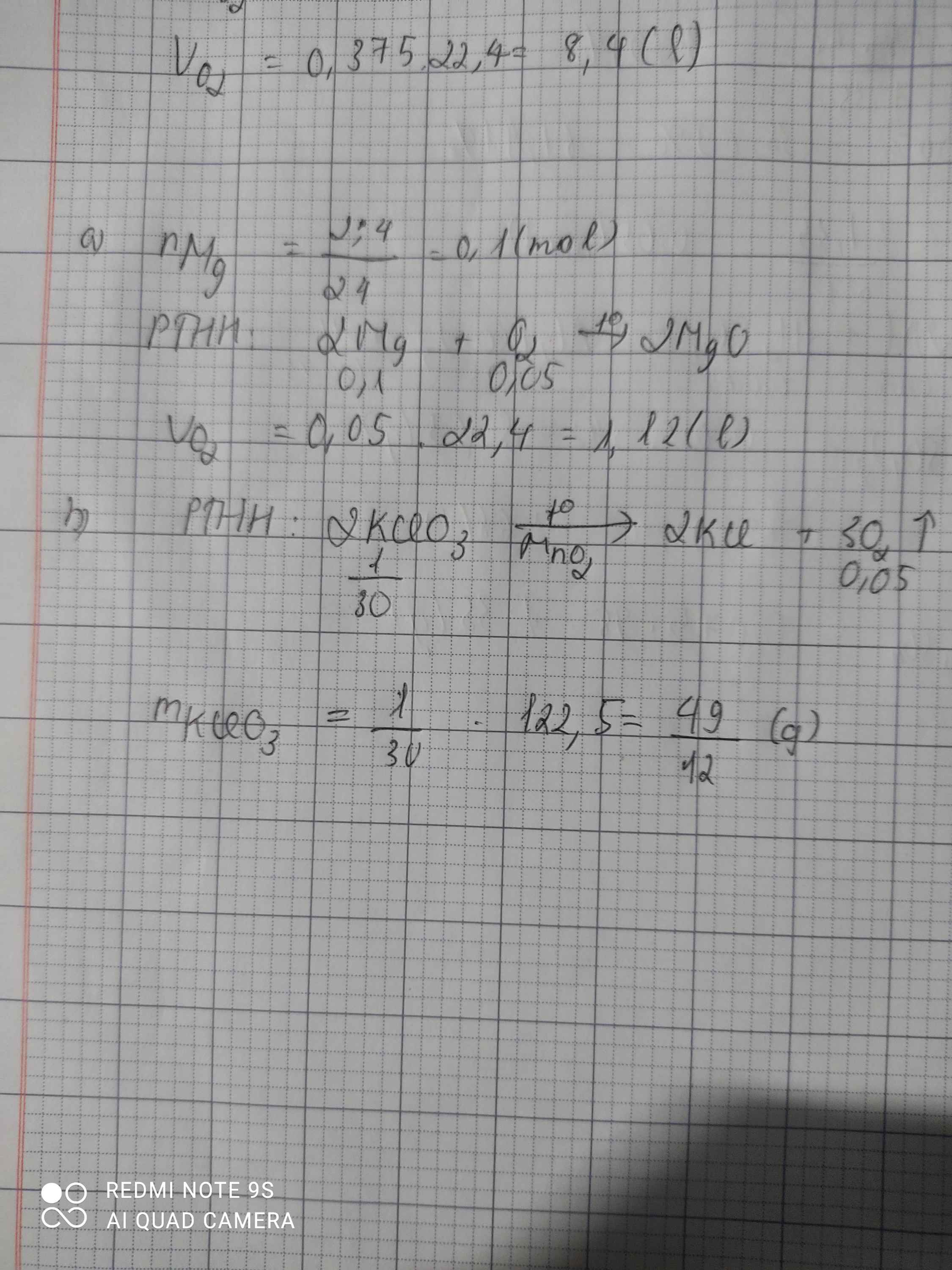

a.\(n_{Cu}=\dfrac{6,4}{64}=0,1mol\)
\(2Cu+O_2\rightarrow\left(t^o\right)2CuO\)
0,1 0,05 ( mol )
\(V_{kk}=\left(0,05.22,4\right).5=5,6l\)
b.\(2KClO_3\rightarrow\left(t^o\right)2KCl+3O_2\)
1/30 0,05 ( mol )
\(m_{KClO_3}=\dfrac{1}{30}.122,5=4,08g\)