K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
Dưới đây là một vài câu hỏi có thể liên quan tới câu hỏi mà bạn gửi lên. Có thể trong đó có câu trả lời mà bạn cần!

9 tháng 5 2018
Đáp án B
X là nguyên tố nhóm IIA (hóa trị II)
Y là nguyên tố nhóm VA (hóa trị III)
Như vậy, công thức hợp chất phải là X3Y2

17 tháng 3 2017
+ có cấu hình e: 1s22s22p6
Mà R → R+ + 1e
Vậy R có cấu hình: 1s22s22p63s1; R có số hiệu nguyên tử = số electron = 11 → Chọn D.

19 tháng 7 2018
Đáp án D
R+ có cấu hình e: 1s22s22p6
Mà R → R+ + 1e
Vậy R có cấu hình: 1s22s22p63s1; R có số hiệu nguyên tử = số electron = 11
→ Chọn D.

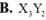



Đáp án A.
Cấu hình electron của X: 1s2 2s22p63s1