Cho 32 gam CuO tác dụng vừa đủ V lỉt dung dịch hỗn hợp 3 axit HCl, H2SO4, HNO3 có nồng độ mol lần lượt là 1,5M, 1M, 0,5M. Tính V.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
0,2--->0,4---->0,2--->0,2
\(V_2=0,2.22,4=4,48\left(l\right)\)
\(V_1=\dfrac{0,4}{0,5}=0,8\left(l\right)\)
b)
\(C_{M\left(ZnCl_2\right)}=\dfrac{0,2}{0,8}=0,25M\)
c)
\(n_{H_2}=0,1\left(mol\right)\); \(n_{CuO}=\dfrac{32}{80}=0,4\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
Xét tỉ lệ: \(\dfrac{0,4}{1}>\dfrac{0,1}{1}\) => CuO dư, H2 hết
PTHH: CuO + H2 --to--> Cu + H2O
0,1<--0,1------>0,1
=> m = 32 - 0,1.80 + 0,1.64 = 30,4 (g)

Chọn A
Gọi nồng độ mol ban đầu của HCl và H 2 S O 4 lần lượt là x và y (M)



100ml = 0,1l
Số mol của dung dịch axit sunfuric
CMH2SO4 = \(\dfrac{n}{V}\Rightarrow n=C_M.V=2.0,1=0,2\left(mol\right)\)
100ml = 0,1l
Số mol của dung dịch bari nitrat
CMBa(NO3)2 = \(\dfrac{n}{V}\Rightarrow n=C_M.V=1.0,1=0,1\left(mol\right)\)
Pt : H2SO4 + Ba(NO3)2 → 2HNO3 + BaSO4\(|\)
1 1 2 1
0,2 0,1 0,2
Lập tỉ số so sánh : \(\dfrac{0,2}{1}>\dfrac{0,1}{1}\)
⇒ H2SO4 dư , Ba(NO3)2 phản ứng hết
⇒ Tính toán dựa vào số mol của Ba(NO3)2
Số mol của axit nitric
nHNO3 = \(\dfrac{0,1.2}{1}=0,2\left(mol\right)\)
Số mol dư của dung dịch axit sunfuric
ndư = nban đầu - nmol
= 0,2 - (0,1. 1)
= 0,1 (mol)
Thể tích của dung dịch sau phản ứng
Vdung dịch sau phản ứng = 0,1 + 0,1
= 0,2 (l)
Nồng độ mol của axit nitric
CMHNO3 = \(\dfrac{n}{V}=\dfrac{0,2}{0,2}=1\left(M\right)\)
Nồng độ mol của dung dịch axit sunfuric
CMH2SO4 = \(\dfrac{n}{V}=\dfrac{0,1}{0,2}=0,5\left(M\right)\)
⇒ Chọn câu : D
Chúc bạn học tốt

Chọn B
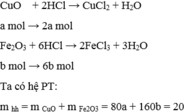
Gọi a là số mol của CuO và b là số mol của F e 2 O 3 có trong 20 gam
hh 200 ml dd HCl 3,5 M => nHCl = 0,2 . 3,5 = 0,7 mol
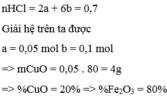
\(n_{HCl} = 1,5V(mol) ; n_{H_2SO_4}= V(mol) ; n_{HNO_3} = 0,5V(mol)\\ n_{CuO} = \dfrac{32}{80} = 0,4(mol)\\ CuO + 2HCl \to CuCl_2 + H_2O\\ CuO + H_2SO_4 \to CuSO_4 + H_2O\\ CuO + 2HNO_3 \to Cu(NO_3)_2 + H_2O\\ n_{CuO} = \dfrac{1}{2}n_{HCl} + n_{H_2SO_4} + \dfrac{1}{2}n_{HNO_3}\\ \Rightarrow 0,4 = 0,5.1,5V + V + 0,5V.0,5\\ \Rightarrow V = 0,2(lít)\)