Đun nóng hỗn hợp gồm 11,2 gam bột sắt và 3,2 gam bột lưu huỳnh thu được chất rắn A. Tính thể tích dung dịch HCl 0,5M vừa đủ để hòa tan hết chất rắn A.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{Al}=\dfrac{8,1}{27}=0,3\left(mol\right)\)
\(n_S=\dfrac{9,6}{32}=0,3\left(mol\right)\)
Do khi hòa tan A vào HCl thu được hỗn hợp khí
=> Trong A chứa H2, H2S
=> Al dư, S hết
PTHH: 2Al + 3S --to--> Al2S3
0,2<--0,3------>0,1
2Al + 6HCl --> 2AlCl3 + 3H2
0,1----------------------->0,15
Al2S3 + 6HCl --> 2AlCl3 + 3H2S
0,1------------------------>0,3
=> \(\overline{M}_X=\dfrac{0,15.2+0,3.34}{0,15+0,3}=\dfrac{70}{3}\left(g/mol\right)\)
=> \(d_{X/H_2}=\dfrac{\dfrac{70}{3}}{2}=\dfrac{35}{3}\)

Fe + S -----> FeS
FeS + 2 HCl ----> FeCl2 + H2S
Fe + 2HCl ----> FeCl2 + H2
a) n(Fe) = 5,6 : 56 = 0,1 ( mol)
n ( S ) = 1,5 : 32 = 0,05 ( mol )
=> sau phản ứng thứ nhất : n(Fe) dư = 0,1 - 0,05 = 0,05 mol ; n(FeS) =n (S ) = 0,05 ( mol)
a) Các chất rắn trong B là: Fe và FeS
Các chất trong dung dịch A là : FeCl2 và HCl dư
b) n(H2 S) = n ( FeS ) = 0,05 ( mol) => V( H2S) = 0,05 x 22,4 = 1,12 ( lit)
n (H2 ) = n(Fe dư) = 0,05 ( mol ) => V( H2) = 1,12 ( lit)

Đáp án B
nCa = 0,28
nHCl = 2nH2SO4
=>0,28.2 = nHCl + 2nH2SO4 => nHCl = 0,28 => nH2SO4 = 0,14
m+21,14 = 11,2 + 0,14.96 + 0,28.35,5 => m = 13,44g => nO = (13,44 - 21,14)/16 = 0,14
Bảo toàn e : 0,28.2 = 0,14.2 + 8nNH4NO3 + 0,04.3 => nNH4NO3 = 0,02
=>mran khan = 0,28.(40 + 62.2) + 0,02.80 = 47,52g
=>B

Gọi x,y là số mol Fe phản ứng, Fe dư
Fe+S\(\rightarrow\)FeS
.x.....x.........x
FeS+2HCl−−−>FeCl2+H2S
.....x....................................x
Fe+2HCl−−−>FeCl2+H2
...y................................y
H2S+Pb(NO3)2−−−>PbS\(\downarrow\)+2HNO3
0,1..............................0,1........
Ta có: \(\dfrac{34x+2y}{x+y}\)=18
=> x=y=0,1
m\(_{Fe}\)bđ=m\(_{Fe}\) pứ + m\(_{Fe}\) dư =0,1.2.56=11,2(g)
m\(_S\)bđ=m\(_S\) pứ + m\(_S\) dư =0,1.32+0,8=4(g)


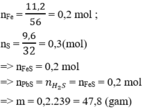

\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\\ n_S=\dfrac{3,2}{32}=0,1\left(mol\right)\)
PTHH: Fe + S --to--> FeS
LTL: \(0,2>0,1\rightarrow\) Fe dư
\(n_{Fe\left(pư\right)}=n_{FeS}=n_S=0,1\left(mol\right)\\ \rightarrow n_{Fe\left(dư\right)}=0,2-0,1=0,1\left(mol\right)\)
PTHH:
FeS + 2HCl ---> FeCl2 + H2
0,1 0,2
Fe + 2HCl ---> FeCl2 + H2
0,1 0,2
\(\rightarrow V_{ddHCl}=\dfrac{0,2+0,2}{0,5}=0,8\left(l\right)\)
\(n_{Fe}=\dfrac{11,2}{56}=0,2mol\)
\(n_S=\dfrac{3,2}{32}=0,1mol\)
\(Fe+S\rightarrow\left(t^o\right)FeS\)
0,2 < 0,1 ( mol )
0,1 0,1 ( mol )
\(FeS+2HCl\rightarrow FeCl_2+H_2S\)
0,1 0,2 ( mol )
\(V_{HCl}=\dfrac{0,2}{0,5}=0,4l\)