Trong 0,1 lít dd KOH 2M có bao nhiêu gam KOH
A. 11,6g B, 13,8g C. 11,2g D. 0,2g
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) mdd KOH sau trộn = mKOH(ban đầu) + mH2O = 11,2 + 169,8 = 181(g)
=> C%dd KOH sau trộn = \(\dfrac{m_{ct}}{m_{dd}}.100\%=\dfrac{11,2}{181}.100\%=6,188\%\)
b) Có : nKOH = 11,2/56 = 0,2(mol)
Lại có : Vdd = m : D = 181 : 1,04 =174 (ml) = 0,174(l)
=> CM của dd KOH thu được = n/V = 0,2/0,174 = 1,15(M)
c) Có 2 cách làm : cách 1 áp dụng sơ đồ đường chéo nhưng ở đâu vẽ k được nên làm cách 2 : kiểu truyền thống :)
Gọi mKOH(thêm vào) = a(g)
Có : mKOH / dd A = \(\dfrac{m_{dd}.C\%}{100\%}=\dfrac{150.5\%}{100\%}=7,5\left(g\right)\)
=> Tổng mKOH sau trộn = mKOH / dd A + mKOH thêm vào = 7,5 + a (g)
=> mdd sau trộn = mdd A + mKOH thêm vào = 150 + a (g)
\Có : C%dd KOH sau trộn= \(\dfrac{m_{ct}}{m_{dd}}.100\%=8,5\%\Rightarrow\dfrac{7,5+a}{150+a}=0,085\)
=> 7,5 + a = 12,75 + 0,085a
=>a = 350/61 (g)
Vậy cần thêm 350/61 g KOH

Khi hòa tan Kalihidroxit vào nước ta thu được dung dịch dung dịch Kali hidroxit
\(C\%_{KOH}=\dfrac{11,2.100}{11,2+169,8}=6,19\%\)
\(\Rightarrow C_{M_{KOH}}=\dfrac{10.6,19.1,04}{56}=1,15\left(M\right)\)
Gọi a là khối lượng KOH cần thêm vào
\(m_{KOH}\left(bđ\right)=\dfrac{5.150}{100}=7,5\left(g\right)\)
\(\Rightarrow m_{KOH}\left(sau\right)=\left(7,5+a\right)\left(g\right)\)
\(m_{ddKOH}\left(sau\right)=\left(150+a\right)\left(g\right)\)
Theo đề, sau khi thêm a gam KOH vào A ta thu được dung dịch có nồng độ là 8,5%
\(\Rightarrow8,5=\dfrac{\left(7,5+a\right).100}{150+a}\)
\(\Rightarrow a=5,74\left(g\right)\)
Vậy cần thêm 5,74 gam KOH.

\(a)Bte:3n_{Fe}+3n_{Al}=n_{Ag}\\ \Leftrightarrow n_{Ag_3}=0,1.3+0,1.3\\ \Leftrightarrow n_{Ag}=0,6mol\\ m_{rắn}=m_{Ag}=0,6.108=64,8g\\ BTNT\left(Ag\right):n_{Ag}=n_{AgNO_3}=0,6mol\\ V_{AgNO_3}=\dfrac{0,6}{2}=0,3l\\ BTNT\left(Al\right):n_{Al}=2n_{Al_2O_3}\\ \Leftrightarrow0,1=2n_{Al_2O_3}\\ \Leftrightarrow n_{Al_2O_3}=0,05mol\\ BTNT\left(Fe\right):n_{Fe}=2n_{Fe_2O_3}\\ \Leftrightarrow0,1=2n_{Fe_2O_3}\\ \Leftrightarrow n_{Fe_2O_3}=0,05mol \\ b=m_{oxit.bazo}=0,05.\left(160+102\right)=13,1g\)

Ta có các phản ứng phân li sau:
H2SO4 = 2H+ + SO42-
0,02 0,04
HNO3 = H+ + NO3-
0,04 0,04 mol
NaOH = Na+ + OH-
0,06 0,06
KOH = K+ + OH-
0,03 0,03 mol
Bản chất của phản ứng giữa 2 dung dịch trên là phản ứng axit - bazo nên:
H+ + OH- = H2O
0,08 0,09
Theo phản ứng (1) thì OH- dư 0,01 mol nên môi trường phản ứng sau phản ứng là môi trường bazo.
Mà [H+].[OH-] = 10-14, nên [H+] = 10-14/10-2 = 10-12, do đó pH của Z = -log(10-12) = 12.
Để trung hòa hết dd Z thì cần dùng 0,01 mol H+, tức là 0,005 mol H2SO4, nên V = 0,005/2 = 0,0025 lít = 2,5 ml.

Phương trình hóa học CaCO3 → CaO + CO2.
a) nCaO = 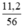 = 0,2 mol.
= 0,2 mol.
Theo PTHH thì nCaCO3 = nCaO = 0,2 (mol)
b) nCaO = 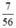 = 0,125 (mol)
= 0,125 (mol)
Theo PTHH thì nCaCO3 = nCaO = 0,125 (mol)
mCaCO3 = M.n = 100.0,125 = 12,5 (g)
c) Theo PTHH thì nCO2 = nCaCO3 = 3,5 (mol)
VCO2 = 22,4.n = 22,4.3,5 = 78,4 (lít)
d) nCO2 = 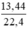 = 0,6 (mol)
= 0,6 (mol)
Theo PTHH nCaO = nCaCO3 = nCO2 = 0,6 (mol)
mCaCO3 = n.M = 0,6.100 = 60 (g)
mCaO = n.M = 0,6.56 = 33,6 (g)

C
C