Cho 10,88gam hỗn hợp gồm Fe, Cu tác dụng hết với 15,62gam khí clo.
a. Tính % theo khối lượng mỗi kim loại.
b. Cho lượng muối thu được tác dụng với dung dịch AgNO3 24%. Tính khối lượng chất kết tủa thu được, khối lượng dung dịch AgNO3 phản ứng.
c. Nếu cho lượng khí clo trên qua 100ml dung dịch NaI aM, tính khối lượng iot sinh ra, giá trị a = ?
d. Cho x gam MnO2 tác dụng với 50ml dung dịch HCl yM để điều chế lượng khí clo trên, tính x, y = ?








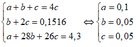

\(a,n_{Cl_2}=\dfrac{15,62}{71}=0,22\left(mol\right)\\ Đặt:n_{Fe}=a\left(mol\right);n_{Cu}=b\left(mol\right)\left(a,b>0\right)\\ 2Fe+3Cl_2\rightarrow\left(t^o\right)2FeCl_3\\ Cu+Cl_2\rightarrow\left(t^o\right)CuCl_2\\ \Rightarrow\left\{{}\begin{matrix}56a+64b=10,88\\1,5a+b=0,22\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,08\\b=0,1\end{matrix}\right.\\ \Rightarrow\%m_{Fe}=\dfrac{0,08.56}{10,88}.100\approx41,176\%\Rightarrow\%m_{Cu}\approx58,824\%\\ b,FeCl_3+3AgNO_3\rightarrow Fe\left(NO_3\right)_3+3AgCl\downarrow\\ CuCl_2+2AgNO_3\rightarrow Cu\left(NO_3\right)_2+2AgCl\\ n_{AgNO_3}=3.0,08+2.0,1=0,44\left(mol\right)\\ m_{AgNO_3}=0,24.170=40,8\left(g\right)\\ m_{ddAgNO_3}=\dfrac{40,8}{24\%}=170\left(g\right)\)
\(c,2NaI+Cl_2\rightarrow2NaCl+I_2\\ n_{NaI}=2.n_{Cl_2}=2.0,22=0,44\left(mol\right)\Rightarrow a=C_{MddNaI}=\dfrac{0,44}{0,1}=4,4\left(M\right)\\ n_{I_2}=n_{Cl_2}=0,22\left(mol\right)\Rightarrow m_{I_2}=254.0,22=55,88\left(g\right)\)
\(d,MnO_2+4HCl_{\left(đặc\right)}\rightarrow\left(t^o\right)MnCl_2+Cl_2+2H_2O\\ n_{MnO_2}=n_{Cl_2}=0,22\left(mol\right)\\ \Rightarrow x=m_{MnO_2}=87.0,22=19,14\left(g\right)\\ n_{HCl}=4.0,22=0,88\left(mol\right)\\ y=C_{MddHCl}=\dfrac{0,88}{0,05}=17,6\left(M\right)\)