Đốt cháy hoàn toàn 5,8g một hợp chất hữu cơ X bằng khí \(O_2\), thu được 6,72 lít khí \(CO_2\) (ở đktc), và 5,4g \(H_2O\). Xác định công thức phân tử và thành phần phần trăm khối lượng của các nguyên tố trong X?
Giúp mk vs ạ mình đang cần gấp thanks trước



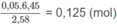
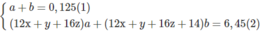
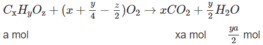
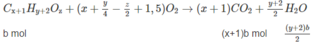
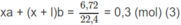
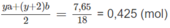
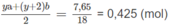
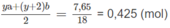
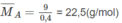
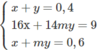

\(n_{CO_2}=\dfrac{6,72}{22,4}=0,3(mol)\\ n_{H_2O}=\dfrac{5,4}{18}=0,3(mol)\)
Bảo toàn C và H: \(n_C=0,3(mol);n_H=0,6(mol)\)
\(\Rightarrow m_C=0,3.12=3,6(g);m_H=0,6.1=0,6(g)\\ \Rightarrow m_X>m_C+m_H\)
Do đó X bao gồm \(O\)
\(\Rightarrow m_O=5,8-3,6-0,6=1,6(g)\\ \Rightarrow n_O=\dfrac{1,6}{16}=0,1(mol)\)
Gọi CT của X là \(C_xH_yO_z\)
\(\Rightarrow x:y:z=0,3:0,6:0,1=3:6:1\\ \Rightarrow CTPT_X:C_3H_6O\)
\(\%_C=\dfrac{36}{58}.100\%=62,07\%\\ \%_H=\dfrac{6}{58}.100\%=10,34\%\\ \%_O=100\%-62,07\%-10,34\%=27,59\%\)
tính % m các nguyên tố trong X nhé