Cho 86,3 gam hỗn hợp X gồm Na, K, Ba và Al2O3 (trong đó oxi chiếm 19,47% về khối lượng) tan hết vào nước thu được dung dịch Y và 13,44 lít H2 (đktc). Cho 3,2 lít dung dịch HCl 0,75M vào dung dịch Y thu được m gam kết tủa. Lấy m gam kết tủa đó cho tan hết trong V mL dung dịch KOH 1,25M. Giá trị tối thiểu của V là
A. 240.
B. 360.
C. 320.
D. 220.



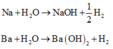
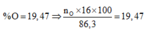
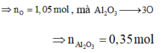
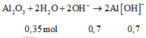
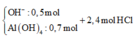
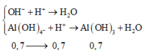
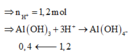
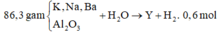

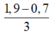
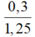

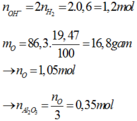
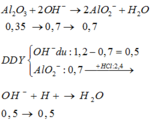
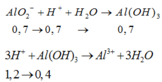
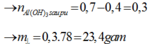
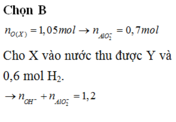

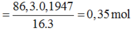


Đáp án A
%mO/X = 86,3×0,1947 = 16,8 gam.
⇒ nO = 1,05 ⇒ nAl2O3 = 0,35 mol.
Ta có ∑nOH– = 2nH2 = 1,2 mol.
⇒ Dung dịch Y chứa nAlO2– = nAl/Al2O3 = 0,7 mol || nOH dư = 0,5 mol.
+ Sau phản ứng trung hòa nH+ = 3,2×0,75 – 0,5 = 1,9 mol
⇒ nAl(OH)3 = 0,7 – 1 , 9 - 0 , 7 3 = 0,3 mol.
+ Cho 0,3 mol Al(OH)3 phản ứng với KOH ta có phản ứng:
Al(OH)3 + KOH → KAlO2 + 2H2O ||⇒ nKOHcần dùng = 0,3.
⇒ VKOH = 0 , 3 1 , 25 = 0,24 lít = 240 ml