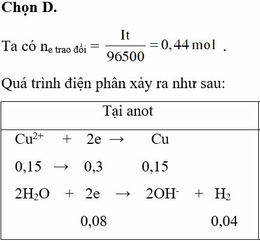
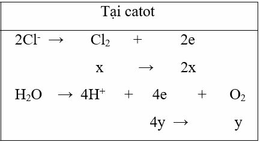
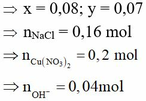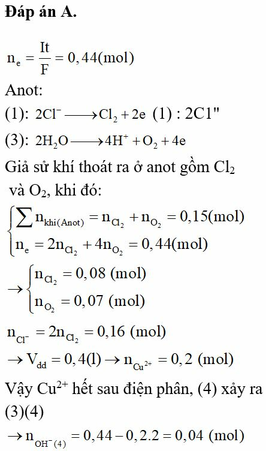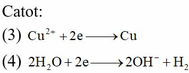Tiến hành điện phân dung dịch chứa NaCl 0,4M và Cu(NO3)2 0,5M bằng điện cực trơ, màng ngăn xốp với cường độ dòng điện không đổi I = 5A trong thời gian 8492 giây thì dừng điện phân, ở anot thoát ra 3,36 lít khí (đktc). Cho m gam bột Fe vào dung dịch sau điện phân, kết thúc phản ứng, thấy khí NO thoát ra (sản phẩm khử duy nhất của N+5) và 0,8m gam rắn không tan. Giá trị của m là
A. 29,4 gam
B. 25,2 gam
C. 16,8 gam
D. 19,6 gam