Nung nóng hỗn hợp X gồm KMnO4, MnO2 và KClO3 sau một thời gian thu được 1,344 lít khí O2 (đktc) và 15,23 gam hỗn hợp rắn Y. Hòa tan hết 15,23 gam hỗn hợp rắn Y cần dùng dung dịch chứa 0,6 mol HCl, thu được 4,48 lít khí Z (đktc). Phần trăm khối lượng của MnO2 trong hỗn hợp X có giá trị gần nhất với giá trị nào sau đây?
A. 30%
B. 20%
C. 25%
D. 40%





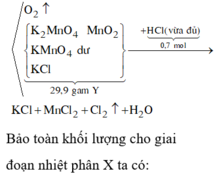



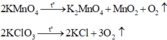
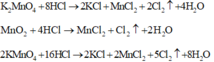
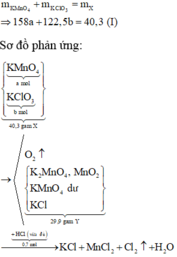
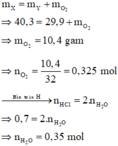

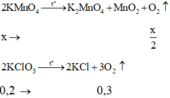
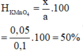

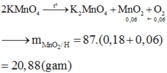


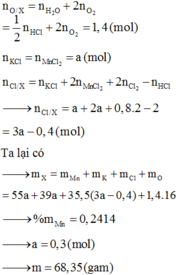

Chọn đáp án B