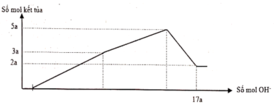
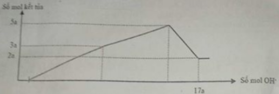
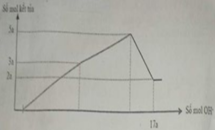
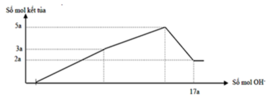
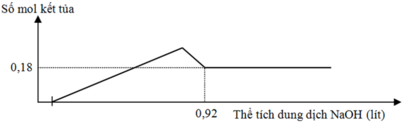
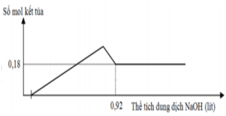
Hòa tan hết 12,060 gam hỗn hợp gồm Mg và Al2O3 trong dung dịch chứa HCl 0,5M và H2SO4 0,1M. Sau khi kết thúc phản ứng thu được dung dịch X. Cho từ từ dung dịch NaOH 1,0M vào dung dịch X, phản ứng được biểu diễn theo đồ thị sau:
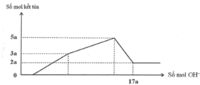
Nếu cho từ từ V ml dung dịch NaOH 0,3M và Ba(OH) 2 0,1M vào dung dịch X, thu được kết tủa lớn nhất. Lấy kết tủa nung trong không khí đến khối lượng không đổi, thu được m gam chất rắn khan. Giá trị của m là
A. 41,940
B. 37,860
C. 48,152
D. 53,125





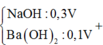





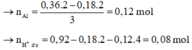

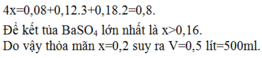
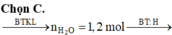
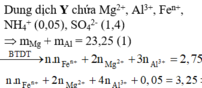
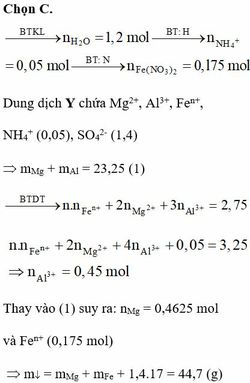

Đáp án A