Điện phân 150 ml dung dịch AgNO3 1M với điện cực trơ trong t giờ, cường độ dòng điện không đổi 2,68A (hiệu suất quá trình điện phân là 100%), thu được chất rắn X, dung dịch Y và khí Z. Cho 12,6 gam Fe vào Y, sau khi các phản ứng kết thúc thu được 14,5 gam hỗn hợp kim loại và khí NO (sản phẩm khử duy nhất của N+5). Giá trị của t là
A. 0,8
B. 0,3
C. 1,0
D. 1,2



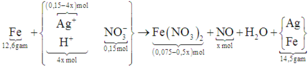

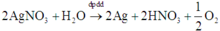
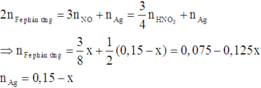
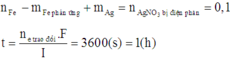
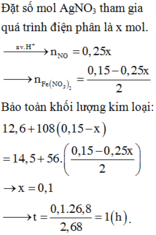

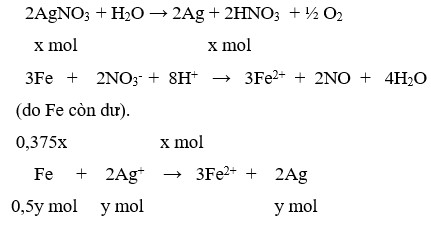
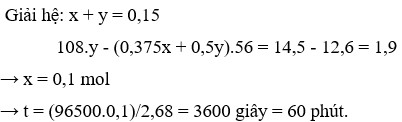

Chọn đáp án C
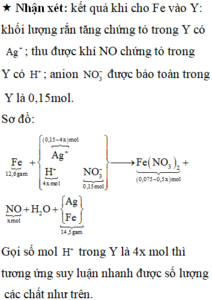
« Nhận xét: kết quả khi cho Fe vào Y: khối lượng rắn tăng chứng tỏ trong Y có Ag+; thu được khí NO chứng tỏ trong Y có H+; anion NO3- được bảo toàn trong Y là 0,15mol.
Gọi số mol H+ trong Y là 4x mol thì tương ứng suy luận nhanh được số lượng các chất như trên.
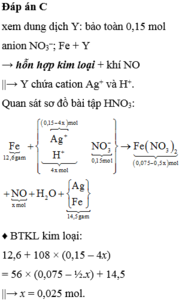
Bảo toàn khối lượng nguyên tố kim loại 2 vế sơ đồ:
12,6 + (0,15 – 4x) x108 =(0,075 – 1/2x)x 56 + 14,5
Giải phương trình được x = 0,045 mol → ∑ne điện phân trao đổi = 4x = 0,1mol.
Áp dụng định luật Faraday ta có thời gian điện phân t = 96500 x 0,1 : 2,68 = 3600 giây ↔ 1 giờ