Cho 8,3g hỗn hợp X gồm Fe và Al vào 1lít dung dịch C u S O 4 0,2 M, sau khi phản ứng xảy ra hoàn toàn thu được 15,68g chất rắn Y gồm 2 kim loại. Thành phần phần trăm theo khối lượng của nhôm trong hỗn hợp X là:
A. 32,53%
B. 53,32%
C. 50%
D. 35,3%
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, 2Al + 3CuSO4 → Al2(SO4)3 + 3Cu
x…………3/2.x
Fe + CuSO4 → FeSO4 + Cu
y……..y
Al phản ứng hết với CuSO4 sau đó Fe mới phản ứng với CuSO4. Vì sau phản ứng thu được rắn Y gồm 2 kim loại nên Al đã tan hết và Fe có thể đã phản ứng 1 phần hoặc chưa phản ứng. 2 kim loại trong Y là Fe và Cu.
⇒ nCu = nCuSO4 = 0,2.1 = 0,2 mol
⇒ mFe dư = mY - mCu = 15,68 - 0,2.64 = 2,88g
Đặt số mol Al ban đầu là x, số mol Fe phản ứng là y, ta có hệ phương trình:
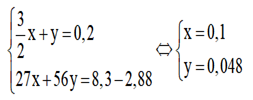
⇒ mAl = 0,1.27 = 2,7g
⇒ %mAl = 2,7/8,3.100 = 32,53%

Đáp án D
Ta có dãy điện hóa: Fe2+/Fe > Fe3+/Fe2+ > Ag+/Ag.
Thu được 2 kim loại ⇒ Fe và Ag ⇒ X chỉ chứa Fe(NO3)2

Gọi $n_{Mg} = a(mol) ; n_{Fe\ pư} = b(mol) ; n_{Fe\ dư} = c(mol)$
$\Rightarrow 24a + 56b + 56c = 10,2(1)$
$Mg + CuCl_2 \to MgCl_2 + Cu$
$Fe + CuCl_2 \to FeCl_2 + Cu$
$n_{Cu} = a + b(mol)$
$\Rightarrow (a + b).64 + 56c = 13,8(2)$
$MgCl_2 + 2KOH \to Mg(OH)_2 + 2KCl$
$FeCl_2 + 2KOH \to Fe(OH)_2 + 2KCl$
$m_{kết\ tủa} = 58a + 90b = 11,1(3)$
Từ (1)(2)(3) suy ra a = 0,075 ; b = 0,075; c = 0,075
$\%m_{Mg} = \dfrac{0,075.24}{10,2}.100\% = 17,65\%$

\(m_{cr}=m_{Fe}=12.8\left(g\right)\)
\(NaOH+Al+H_2O\rightarrow NaAlO_2+\dfrac{3}{2}H_2\)
\(m_{Al}=m_{hh}-m_{Fe}=18.2-12.8=5.4\left(g\right)\)
\(\%m_{Al}=\dfrac{5.4}{18.2}\cdot100\%=29.67\%\)

Đáp án : B
Z + AgNO3 -> NO => H+ dư , NO3- hết ; Z có Fe2+
Kết tủa gồm : nAgCl = nHCl = 1,9 mol => nAg = 0,075 mol
Bảo toàn e : nFe2+ = 3nNO + nAg = 0,15 mol
, nH+ dư = 4nNO = 0,1 mol
Trong dung dịch Z gồm : Al3+ ; Fe2+ ; Fe3+ ; H+ ; Cl-
Bảo toàn điện tích : nAl + 2nFe2+ + 3nFe+ + nH+ = nCl- => nFe3+ = 0,2 mol
=> nFe (Y) = 0,35 mol
Bảo toàn H : nH2O = ½ nH+ pứ = 0,975 mol
Bảo toàn O : nO(Y) + nHNO3 = nO(T) + nH2O
=> nO(Y) = 0,8 mol
Ta có : mY = mAl + mnguyên tố Fe + mO + mN
=> nN = 0,2 mol => nFe(NO3)2 = 0,1 mol
=> %mFe(NO3)2 = 41,57%

Đáp án C
(1) Mg + 2Ag+ à Mg2+ + 2Ag
(2) Fe + 2Ag+ à Fe2+ + 2Ag
(3) Fe2+ + Ag+ à Fe3+ + Ag
Vì Chất rắn Y gồm 2 kim loại => đó là Ag và Fe => không thể xảy ra (3) và Ag+ phải hết
=> X gồm Mg2+ và Fe2+
2 A l + 3 C u S O 4 → A l 2 S O 4 3 + 3 C u
x…………3/2.x
F e + C u S O 4 → F e S O 4 + C u
y……..y
Al phản ứng hết với C u S O 4 sau đó Fe mới phản ứng với C u S O 4 . Vì sau phản ứng thu được rắn Y gồm 2 kim loại nên Al đã tan hết và Fe có thể đã phản ứng 1 phần hoặc chưa phản ứng. 2 kim loại trong Y là Fe và Cu.
⇒ n C u = n C u S O 4 = 0,2.1 = 0,2 mol
⇒ m F e dư = m Y - m C u = 15,68 - 0,2.64 = 2,88g
Đặt số mol Al ban đầu là x, số mol Fe phản ứng là y, ta có hệ phương trình:
⇒ m A l = 0,1.27 = 2,7g
⇒ % m A l = 2,7/8,3.100 = 32,53%
⇒ Chọn A.