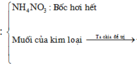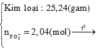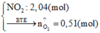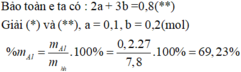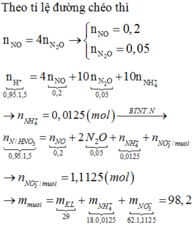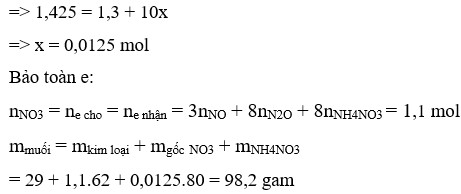Cho 5,6 lít hỗn hợp X gồm: C l 2 , O 2 (ở đktc, tỉ khối so với He là 13,85) phản ứng vừa đủ với 15,5 gam hỗn hợp Y gồm: Al, Cu thu được a gam chất rắn. Xác định % khối lượng các chất trong Y.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



a)
Gọi số mol O2, Cl2 là a, b (mol)
=> \(\left\{{}\begin{matrix}a+b=\dfrac{5,6}{22,4}=0,25\\\overline{M}=\dfrac{32a+71b}{a+b}=23,8.2=47,6\end{matrix}\right.\)
=> a = 0,15; b = 0,1
Gọi số mol Mg, Al là x, y (mol)
=> 24x + 27y = 7,8 (1)
Mg0 - 2e --> Mg+2
x---->2x
Al0 - 3e --> Al+3
y--->3y
O20 + 4e --> 2O-2
0,15->0,6
Cl20 + 2e --> 2Cl-
0,1-->0,2
Bảo toàn e: 2x + 3y = 0,8 (2)
(1)(2) => x = 0,1; y = 0,2
=> \(\left\{{}\begin{matrix}m_{Mg}=0,1.24=2,4\left(g\right)\\m_{Al}=0,2.27=5,4\left(g\right)\end{matrix}\right.\)
b) Gọi công thức chung của 2 halogen là \(\overline{T_2}\)
\(m_{\overline{T_2}}=54-7,8=46,2\left(g\right)\)
Mg0 - 2e --> Mg+2
0,1---->0,2
Al0 - 3e --> Al+3
0,2-->0,6
\(\overline{T_2}+2e\rightarrow2\overline{T}^-\)
Bảo toàn e: \(n_{\overline{T_2}}=0,4\left(mol\right)\)
=> \(M_{\overline{T_2}}=\dfrac{46,2}{0,4}=115,5\left(g/mol\right)\)
Mà 2 halogen ở 2 chu kì liên tiếp
=> 2 halogen là Cl2, Br2
\(\overline{M}_Z=115,5\left(g/mol\right)\)
=> \(d_{Z/H_2}=\dfrac{115,5}{2}=57,75\)

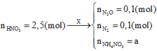
Có n Z = 0,2 mol ; MZ = 36 = ½(MNO + MN2O)
=> nNO =nN2O = 0,1 mol nHNO3=2,5 mol.
Giả sử sản phẩm khử có NH4NO3
=> n HNO3 = 10nN2O + 12nNO + 10nNH4NO3
=> n NH4NO3 = 0,03 mol
=> n NO3 trong muối kim lọai = 2,5 -0,1.2 – 0,1.2 – 0,03.2 =2,04 mol
Khi nhiệt phân muối thì NH4NO3 tạo N2O và H2O bay đi,
chỉ còn caccs oxit kim loại => Ta thấy 2.nO (oxit)= n kim loại.
Điện tích = ne trao đổi = 0.1.8 + 0,1.10 + 0,03.8=2,04 mol
=> no =1,02 mol
=> a-b = mNO3 trong muối KL + m NH4NO3 – mO
= 2,04.62 + 0,03.80 – 1,02.16 =112,56g
Gần nhất với giá trị 110,50g =>A

Có n Z = 0,2 mol ; MZ = 36 = 1/2(MNO + MN2O)
=> nNO =nN2O = 0,1 mol nHNO3=2,5 mol.
Giả sử sản phẩm khử có NH4NO3
=> n HNO3 = 10nN2O + 12nNO + 10nNH4NO3
=> n NH4NO3 = 0,03 mol => n NO3
trong muối kim lọai = 2,5 -0,1.2 – 0,1.2 – 0,03.2 =2,04 mol
Khi nhiệt phân muối thì NH4NO3 tạo N2O và H2O bay đi,
chỉ còn caccs oxit kim loại => Ta thấy 2.nO (oxit)= n kim loại.
Điện tích = ne trao đổi = 0.1.8 + 0,1.10 + 0,03.8=2,04 mol
=> no =1,02 mol
=> a-b = mNO3
trong muối KL + m NH4NO3 – mO = 2,04.62 + 0,03.80 – 1,02.16 =112,56g
Gần nhất với giá trị 110,50g =>A

nHNO3 ban đầu = 1,425
MX = 32,8; Sử dụng sơ đồ đường chéo ⇒ n NO = 0,2 ; n N2O = 0,05
Ta có nNO3- trong muối kl = ne = 8nN2O + 8nNH4NO3
Bảo toàn nguyên tố N: nHNO3 ban đầu = n NO + 2n N2O + 2n NH4NO3 + n NO3- trong muối KL
⇒ nHNO3 ban đầu = 4 nNO + 10 nN2O + 10 nNH4NO3
⇒ nNH4NO3 = 0,0125
⇒ nNO3-/muối KL= 1,1
⇒ m = mNO3-/muối kl + mKL + mNH4NO3 = 1,1.62 +29 + 0,0125.80 = 98,2g
Đáp án A.

nHNO3 ban đầu = 1,425
MX = 32,8; Sử dụng sơ đồ đường chéo ⇒ n NO = 0,2 ; n N2O = 0,05
Ta có nNO3- trong muối kl = ne = 8nN2O + 8nNH4NO3
Bảo toàn nguyên tố N: nHNO3 ban đầu = n NO + 2n N2O + 2n NH4NO3 + n NO3- trong muối KL
⇒ nHNO3 ban đầu = 4 nNO + 10 nN2O + 10 nNH4NO3
⇒ nNH4NO3 = 0,0125
⇒ nNO3-/muối KL= 1,1
⇒ m = mNO3-/muối kl + mKL + mNH4NO3 = 1,1.62 +29 + 0,0125.80 = 98,2g
Đáp án A.