Hai bình chứa hỗn hợp bột đồng và bột sắt. Trong bình thứ 1, khối lượng bột sắt bằng 20% khối lượng hỗn hợp. Trong bình thứ 2 khối lượng bột đồng bằng 60% khối lượng hỗn hợp. Người ta trộn hỗn hợp trong 2 bình trên với nhau, khi đó khối lượng hỗn hợp mới tạo thành là 250g và khối lượng bột sắt bằng 28% khối lượng hỗn hợp. Tính khối lượng bột đồng và khối lượng bột sắt trong mỗi bình ban đầu.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)
Theo ĐLBTKL: \(m_{Fe\left(bđ\right)}+m_{O_2}=m_X\)
=> \(m_{O_2}=26,4-20=6,4\left(g\right)\)
=> \(n_{O_2}=\dfrac{6,4}{32}=0,2\left(mol\right)\Rightarrow V=0,2.22,4=4,48\left(l\right)\)
b)
PTHH: 3Fe + 2O2 --to--> Fe3O4
0,2------->0,1
=> \(\%m_{Fe_3O_4}=\dfrac{0,1.232}{26,4}.100\%=87,88\%\)
c)
- Nếu dùng KClO3
PTHH: 2KClO3 --to--> 2KCl + 3O2
\(\dfrac{0,4}{3}\)<-----------------0,2
=> \(m_{KClO_3}=\dfrac{0,4}{3}.122,5=\dfrac{49}{3}\left(g\right)\)
- Nếu dùng KMnO4:
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
0,4<--------------------------------0,2
=> \(m_{KMnO_4}=0,4.158=63,2\left(g\right)\)

Gọi nFe = x mol, theo PT ⇒ nS (1) = nFe = x mol
Gọi nAl = y mol, theo PT ⇒ nS (2) = 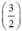 . nAl =
. nAl = 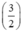 . y mol
. y mol
⇒ nS = x + 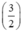 . y = 0,04 mol.
. y = 0,04 mol.
mhh = 56x + 27y = 1,1.
Giải hệ phương trình ta có x = 0,01 mol, y= 0,02 mol.
Tỉ lệ % sắt và nhôm trong hỗn hợp theo lượng chất ( theo số mol là):
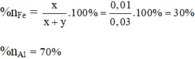
Tỉ lệ phần trăm của sắt và nhôm trong hỗn hợp theo khối lượng chất:
mAl = 0,02 x 27 = 0,54g
mFe = 0,01 x 56 = 0,56g.
%mAl = 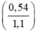 × 100% = 49,09%
× 100% = 49,09%
%mFe = 100% - 49,09% = 50,91%

Fe + S → FeS
x x (mol)
2Al + 3S → t ° Al 2 S 3
y 3y/2(mol)
Đặt số mol Fe, Al lần lượt là x,y ta có hệ phương trình:
56x + 27y = 1,1
(x +3y/2).32 = 1,28
Giải ra x = 0,01 và y = 0,02
% n Fe = 0,01/0,03 x 100% = 33,33%; % n Al = 100 - 33,33% = 66,667%
% m Fe = 56.0,01/1,1 x 100% = 50,90%; % m Al = 100 - 50,90 = 49,1 (%)

bài 1:
ta có phương trình cân bằng nhiệt
Qtỏa=Qthu
\(\Leftrightarrow m_1C_1\left(t_1-t\right)=m_2C_2\left(t-t_2\right)\)
mà hai chất đều là nước nên hai C bằng nhau nên:
\(m_1\left(100-30\right)=m_2\left(30-10\right)\Leftrightarrow70m_1=20m_2\)
mà m1+m2=27kg \(\Rightarrow m_2=27-m_1\)
vì vậy nên ta có;
70m1=20(27-m1)
giải phương trình ta có :
m1=6kg \(\Rightarrow\) m2=21kg
bài 2:
gọi m1,m2,m3,m4 lần lượt là khối lượng của nhôm,sắt,đồng và nước
t1,t2,t3,t4 lần lượt là nhiệt độ của nhôm,sắt,đồng và nước
ta có phương trình cân bằng nhiệt:
Qtỏa=Qthu
\(\Leftrightarrow Q_1+Q_2=Q_3+Q_4\)
\(\Leftrightarrow m_1C_1\left(t_1-t\right)+m_2C_2\left(t_2-t\right)=m_3C_3\left(t-t_3\right)+m_4C_4\left(t-t_4\right)\)
\(\Leftrightarrow880m_1\left(200-20\right)+460m_2\left(200-20\right)=380\cdot0.2\left(20-10\right)+4200\cdot2\cdot\left(20-10\right)\)
\(\Leftrightarrow158400m_1+82800m_2=84760\)
mà m1+m2=0.9\(\Rightarrow m_2=0.9-m_1\)nên:
158400m1+ 82800(0.9-m1)=84760
giải phương trình ta có m1=0.14kg\(\Rightarrow m_2=0.75kg\)
bài 3:
ta có phương trình cân bằng nhiệt:
Qtỏa=Qthu
\(\Leftrightarrow mC\left(t_1-t\right)=mC\left(t-t_2\right)\)
mà t1=2t2
\(\Rightarrow2t_2-30=30-t_2\)
giải phương trình ta có t2=20*C \(\Rightarrow t_1=40\)*C
bài 1:
ta có phương trình cân bằng nhiệt
Qtỏa=Qthu
mà hai chất đều là nước nên hai C bằng nhau nên:
mà m1+m2=27kg
vì vậy nên ta có;
70m1=20(27-m1)
giải phương trình ta có :
m1=6kg m2=21kg
bài 2:
gọi m1,m2,m3,m4 lần lượt là khối lượng của nhôm,sắt,đồng và nước
t1,t2,t3,t4 lần lượt là nhiệt độ của nhôm,sắt,đồng và nước
ta có phương trình cân bằng nhiệt:
Qtỏa=Qthu

Đáp án C.
Fe + CuSO 4 → FeSO 4 + Cu
n Fe = x mol
Khối lượng Fe phản ứng (cũng là khối lượng sắt trong hỗn hợp đầu) là 56x. Khối lượng Cu sinh ra 64x.
CuSO 4 dư nên chất rắn sau phản ứng là đồng :
10 - 56x + 64x = 11 → x = 1/8 mol
m Fe trong hỗn hợp đầu là: 56 x 1/8 = 7g
% m Fe = 7/10 x 100% = 70%
% m C u = 100% - 70% = 30%

Bài 9:
Gọi CTHH của A là NxOy
Ta có: \(\dfrac{m_O}{m_N}=\dfrac{12}{7}\Leftrightarrow\dfrac{16.y}{14.x}=\dfrac{12}{7}\Leftrightarrow\dfrac{y}{x}=\dfrac{12}{7}:\dfrac{16}{14}=\dfrac{12}{7}\cdot\dfrac{14}{16}=\dfrac{3}{2}\)
\(\Rightarrow\left\{{}\begin{matrix}x=2\\y=3\end{matrix}\right.\)
Vậy CTHH của A là N2O3
PTK = 14.2 + 16.3 = 76 (đvC)
Bài 10:
- Lấy nam châm hút bột sắt ra khỏi hỗn hợp
- Đổ hh gồm nhôm và muối vào nước rồi khuấy đều
- Lọc lấy nhôm ra khỏi dd nước muối
- Đun nước muối cho đến khi nước bay hơi hết, còn lại muối kết tinh

Đáp án A.
nS = 0,4 (mol)
=> mhh = mFe + mAl
Bảo toàn electron: 2nFe+ 3nAl = 2nS
=> 56nFe + 27 nAl = 11 ; 2nFe + 3nAl = 2.0,4
=> nFe = 0,1, nAl = 0,2=> mFe = 0,1.56 = 5,6 (gam)

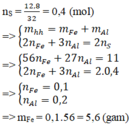

Lời giải:
Gọi khối lượng bột sắt và bột đồng trong bình 1 và bình 2 lần lượt là $(a_1,b_1); (a_2, b_2)$ (g)
Theo bài ra ta có:
\(\left\{\begin{matrix} a_1=0,2(a_1+b_1)(1)\\ b_2=0,6(a_2+b_2)(2)\\ a_1+b_1+a_2+b_2=250\\ a_1+a_2=0,28(a_1+b_1+a_2+b_2)\end{matrix}\right.\)
\(\Leftrightarrow \left\{\begin{matrix} a_1=0,2(a_1+b_1)\\ a_2=0,4(a_2+b_2)\\ a_1+b_1+a_2+b_2=250\\ a_1+a_2=0,28.250=70\end{matrix}\right.\)\(\Rightarrow \left\{\begin{matrix} \frac{a_1}{0,2}+\frac{a_2}{0,4}=250\\ a_1+a_2=70\end{matrix}\right.\Rightarrow \left\{\begin{matrix} a_1=30\\ a_2=40\end{matrix}\right.\) (g)
Kết hợp với $(1)$ và $(2)$ suy ra:
$b_1=4a_1=120$ (g)
$b_2=\frac{3}{2}a_2=60$ (g)
Vậy.......