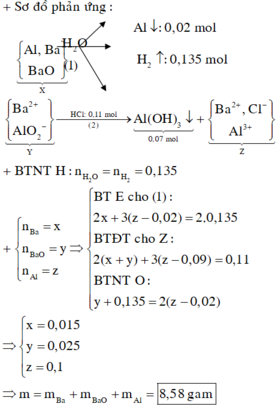
Cho m gam hỗn hợp X gồm Ba, BaO, Al vào nước dư, phản ứng xong, thu được 0,135 mol hiđro, dung dịch Y và 0,54 gam chất rắn không tan. Cho từ từ 110 ml dung dịch HCl 1M vào Y, phản ứng xong, thu được 5,46 gam kết tủa. Viết các phương trình phản ứng xảy ra và tính giá trị của m.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi x, y lần lượt là số mol Ba, BaO
Hòa vào nước tạo 2.(x+y) mol OH-
Al còn dư suy ra số mol Al phản ứng bằng số mol OH- bằng 2(x+y)nH2 = nBa + 1,5nAl = x + 1,5.2.(x+y) = 0,135 (1)
nHCl = 0,11
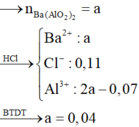
ta có công thức:3nKt + nH+ = 4nAlO2-
=> nAlO2- = 0,08 = n Al phản ứng = 2(x+y) (2) Từ (1,2) => x=0,015=Ba; y=0,025=BaO
Al phản ứng=0,08
m = Ba + BaO + Al pư + Al dư = 8,58g => Đap an C

nAl dư = 0,54/27=0,02
Al(OH)4- + H+ -> Al(OH)3+H2O
x x x
Al(OH)3+3H+ -> Al3+ + 3H2O
0,11-x
Đặt nAl(OH)4- = x
Ta có : x-(0,11-x)/3=0,07 => x=0,08 => nAl pư = 0,08
nH2 = nBa+3/2nAl => nBa = 0,015
=> nBaO=(nAl-2nBa)/2=0,025
=>m=0,1.27+0,015.137+0,025.153=8,58g
=>C

Em tham khảo nhé !
Đặt nAl = a và nFe = b
—> 27a + 56b = 3,28 (1)
nHCl = 0,5 và nNaOH = 0,65
—> nNaCl = 0,5
TH1: Nếu kết tủa vẫn còn Al(OH)3 —> nNaAlO2 = 0,65 – 0,5 = 0,15
Kết tủa gồm Fe(OH)2 (b) và Al(OH)3 (a – 0,15)
Nung ngoài không khí —> Al2O3 (a – 0,15)/2 và Fe2O3 (b/2)
m rắn = 102(a – 0,15)/2 + 160b/2 = 1,6 (2)
(1)(2) —> Vô nghiệm, loại
TH2: Kết tủa chỉ có Fe(OH)2 (b mol)
—> m rắn = 160b/2 = 1,6 (3)
(1)(3) —> a = 0,08 và b = 0,02
—> %Al = 65,85% và %Fe = 34,15%

PTHH: \(Na_2O+H_2O\rightarrow2NaOH\) (1)
\(Al_2O_3+2NaOH\rightarrow2NaAlO_2+H_2O\) (2)
\(NaAlO_2+4HCl\rightarrow NaCl+AlCl_3+2H_2O\) (3)
\(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\) (4)
Ta có: \(\left\{{}\begin{matrix}n_{Al_2O_3\left(dư\right)}=\dfrac{2,04}{102}=0,02\left(mol\right)\\\Sigma n_{HCl}=0,52\cdot1=0,52\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}\Sigma n_{Al_2O_3}=0,22\left(mol\right)\\n_{Na_2O}=0,2\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{hh}=0,22\cdot102+0,2\cdot62=34,84\left(g\right)\)

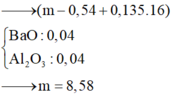



ban ơi bạn sử dụng pp gì để giải vậy
m=8,58 nha mấy bạn nhưng mình ko biết cách trình bày