Nung 1026g hỗn hợp X chứa 49,51% CaOCl2, 28,85% Ca(ClO)2, và 21,64% CaCl2 thu được chất
rắn Y chỉ có canxi clorua và canxi clorat.
a) Viết các phương trình hóa học của phản ứng xảy ra.
b) Tính % khối lượng của CaCl2 trong hỗn hợp Y.
c) Nung hỗn hợp Y tới phản ứng hoàn toàn, thu được chất rắn chỉ có một muối duy nhất và V lít khí Z (ở
đktc). Tính giá trị của V.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

CO2 + Ca(OH)2 → CaCO3↓ + H2O
0,34 ←0,34
CO + O(Oxit) → CO2
Nhận thấy:
nO = nCO2
mX = mO (oxit) + mY
=> mY = 37,68 – 16 . 0,34 = 32,24g

Bài giải:
Câu 1:
a.
Phương trình hóa học :
CaCO3to→CaO+CO2↑CaCO3→toCaO+CO2↑
MgCO3to→MgO+CO2↑MgCO3→toMgO+CO2↑
Phương trình tính khối lượng :
mđolomit=moxit+mCO2mđolomit=moxit+mCO2
b.
Từ câu bb , ta có :
−mđolomit=moxit+mCO2−mđolomit=moxit+mCO2
⇔mđolomit=104+88=192(kg)

a)
$Cu(OH)_2 \xrightarrow{t^o} CuO + H_2O$
$2Fe(OH)_3 \xrightarrow{t^o} Fe_2O_3 + 3H_2O$
Vì theo bảo toàn khối lượng :
$m_{hh} = m_{oxit} + m_{H_2O}$
mà $m_{H_2O} > 0$ nên $m_{hh} > m_{oxit}$
Do đó khối lượng rắn giảm.
b)
Gọi $n_{Cu(OH)_2} = a ; n_{Fe(OH)_3} = b$
$\Rightarrow 98a + 107b = 6,06(1)$
Theo PTHH :
$m_{cr} = 80a + 80b = 4,8(2)$
Từ (1)(2) suy ra a = 0,04; b = 0,02
Suy ra :
$\%m_{Cu(OH)_2} = \dfrac{0,04.98}{6,06}.100\% = 64,67\%$
$\%m_{Fe(OH)_3} = 35,33\%$
\(n_{Cu\left(OH\right)_2}=a\left(mol\right),n_{Fe\left(OH\right)_3}=b\left(mol\right)\)
\(m_{hh}=98a+107b=6.06\left(g\right)\left(1\right)\)
\(Cu\left(OH\right)_2\underrightarrow{^{^{t^0}}}CuO+H_2O\)
\(a............a\)
\(2Fe\left(OH\right)_3\underrightarrow{^{^{t^0}}}Fe_2O_3+3H_2O\)
\(b............0.5b\)
\(m_{Cr}=80a+0.5b\cdot160=4.8\left(g\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.04,b=0.02\)
\(\%Cu\left(OH\right)_2=\dfrac{0.04\cdot98}{6.06}\cdot100\%=64.68\%\)
\(\%Fe\left(OH\right)_3=35.32\%\)

a.
BTKL ta có mX = mY => nX . MX = nY . mY
MX / My = nY / mY =0.75
Đặt nX = 1 mol => nY = 0,75 mol => nH2 phản ứng = 1 – 0,75 = 0,25mol
* TH hidrocacbon là anken: n anken = n H2 = 0,25 mol => n H2 trong X = 0,75 => M = (6,75 – 0,75 . 2)/0,25 = 21 (loại) * TH là ankin: => n akin = 0,25/2 = 0,125 => n H2 trong X = 0,875 mol => M = (6,75 – 0,875 . 2)/0,125 = 40 =>C3H4
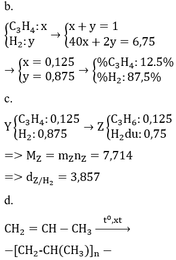


a) mCaCO3 = mCaO + mCO2
b) Khối lượng của CaCO3 đã phản ứng:
140 + 110 = 250 kg
Tỉ lệ phần trăm khối lượng CaCO3 chứa trong đá vôi:
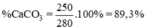


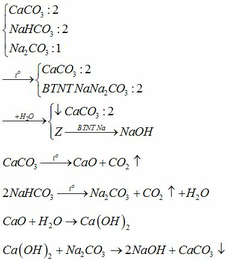

a, \(CaOCl_2\underrightarrow{^{to}}CaCl_2+\frac{1}{2}O_2\)
\(3Ca\left(ClO\right)_2\underrightarrow{^{to}}2CaCl_2+Ca\left(ClO_3\right)_2\)
b,\(m_{CaOCl2}=507,9726\left(g\right)\Rightarrow n_{CaOCl2}=4\left(mol\right)\)
\(m_{Ca\left(OCl\right)2}=296,001\left(g\right)\Rightarrow n_{Ca\left(OCl\right)2}=2\left(mol\right)\)
\(m_{CaCl2}=222,0,264\left(g\right)\Rightarrow n_{CaCl2}=2\left(mol\right)\)
\(\Rightarrow Y\left\{{}\begin{matrix}4+\frac{4}{3}+2=\frac{22}{3}\left(mol\right)CaCl_2\\\frac{2}{3}\left(mol\right)Ca\left(ClO_3\right)_2\end{matrix}\right.\)
\(\%_{CaCl2}=\frac{\frac{22}{3}.111.100}{\frac{22}{3}.111+\frac{2}{3}.207}=85,5\%\)
c,\(Ca\left(ClO_3\right)_2\underrightarrow{^{to}}CaCl_2+3O_2\)
___2_____________________6
\(\Rightarrow V=6.22,4=134,4\left(l\right)\)