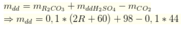cho 6,75 g một kim loại M chưa rõ hóa trị vào cốc đựng 392g dd H2SO4 10%,sau khi miếng kim loại tan hết thấy trong cốc dung dịch vẫn trong suốt và còn dd H2SO4 dư có nồng độ 0,62%.Xác định tên kim loại trên
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án B
Đặt công thức muối cacbonat kim loại là M2CO3
M2CO3+ H2SO4 → M2SO4 + CO2+ H2O
Giả sử n M 2 C O 3 = 1 mol
→ n H 2 S O 4 = n M 2 S O 4 = n C O 2 = 1mol
→ m H 2 S O 4 = 98 gam; m M 2 S O 4 = 2M+96 gam;
m C O 2 = 44 gam; m d d H 2 S O 4 10 % =980 g
Ta có: mdd sau pứ = m M 2 C O 3 + m d d H 2 S O 4 - m C O 2
=2M + 60+980-44= 2M+996 (gam)
C % M 2 S O 4 = 2 M + 96 2 M + 996 . 100 % = 13 , 63 % → M = 23 → M l à N a

gọi dd muối CO3 là ACO3
ACO3 +H2SO4 -->ASO4 +CO2+H2O
giả sử có 1 mol ACO3
=>mACO3= MA +60(g)
theo PTHH : nH2SO4=nACO3=1(mol)
=>mdd H2SO4=1.98.100/20=490(g)
nASO4=nACO3=1(mol)
=>mASO4=MA +96(g)
nCO2=nACO3=1(mol)
=>mCO2=44(g)
=>\(\dfrac{MA+96}{MA+60+490-44}\).100=24,91
giải ra ta được MA=40(g/mol0
=>ACO3:CaCO3
ta có pthh: ACO3 +H2SO4--ASO4+H2O+CO2
(A+60)g......98g.......(A+96)g..........44g
mdd H2SO4=(98.100):20=490g
mdd muối sau phản ứng=(A+60)+490-44= (A+506)g
theo đê bài ta có:C% ASO4=(A+96).100:A+506
suy ra A=40 CÓ: CTHH :CACO3

nH2SO4 ban đầu = 0,25mol
nH2SO4 dư = 0,15
=> nH2SO4 phản ứng = 0,1mol
=> A dư
=> nA > 0,1
MA < 10
=> A là Be

\(n_{H_2}=\dfrac{1.12}{22.4}=0.05\left(mol\right)\)
\(2A+2nH_2O\rightarrow2A\left(OH\right)_n+nH_2\)
\(\dfrac{0.1}{n}........................0.05\)
\(M_A=\dfrac{3.9}{\dfrac{0.1}{n}}=39n\)
Với : \(n=1\rightarrow A=39\)
\(A:K\)
\(m_{KOH}=0.1\cdot56=5.6\left(g\right)\)
\(m_{ddX}=3.9+46.2-0.05\cdot2=50\left(g\right)\)
\(C\%_{KOH}=\dfrac{5.6}{50}\cdot100\%=11.2\%\)
\(b.\)
\(K_2O+H_2O\rightarrow2KOH\)
\(0.1....................0.2\)
\(m_{KOH}=0.2\cdot56=11.2\left(g\right)\)
\(m_{dd_X}=\dfrac{11.2}{28\%\%}=40\left(g\right)\)

\(n_{Mg}=\dfrac{13.44}{24}=0.56\left(mol\right)\)
TN1 :
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(0.56................................0.56\)
TN2 :
\(MCO_3+H_2SO_4\rightarrow MSO_4+CO_2+H_2O\)
\(x............................x\)
Vì cân thăng bằng nên :
\(m_{Mg}-m_{H_2}=m_{MCO_3}-m_{CO_2}\)
\(\Rightarrow13.44-0.56\cdot2=22-44x\)
\(\Rightarrow x=0.22\)
\(M_{MCO_3}=\dfrac{22}{0.22}=100\left(g\text{/}mol\right)\)
\(\Rightarrow M=100-60=40\left(g\text{/}mol\right)\)
\(M:Ca\)

R(III) => CTTQ oxit tạo từ R: R2O3
\(R_2O_3+3H_2SO_4\rightarrow R_2\left(SO_4\right)_3+3H_2O\\ m_{ddsau}=16+384=400\left(g\right)\\ m_{muối}=10\%.400=40\left(g\right)\\ Ta.có:\dfrac{16}{2M_R+48}=\dfrac{40}{2M_R+288}\\ \Leftrightarrow80M_R-32M_R=16.288-40.48\\ \Leftrightarrow48M_R=2688\\ \Leftrightarrow M_R=\dfrac{2688}{48}=56\left(\dfrac{g}{mol}\right)\)
Vậy R(III) cần tìm là sắt (Fe=56)
\(n_{R_2O_3}=\dfrac{16}{2R+48}mol\\ n_{R_2\left(SO_4\right)_3}=\dfrac{\left(384+16\right).10}{100\cdot\left(2R+288\right)}=\dfrac{4000}{200R+28800}mol\\ R_2O_3+3H_2SO_4\rightarrow R_2\left(SO_4\right)_3+3H_2O\\ \Rightarrow n_{R_2O_3}=n_{R_2\left(SO_4\right)_3}\\ \Leftrightarrow\dfrac{16}{2R+48}=\dfrac{4000}{200R+28800}\\ \Leftrightarrow R=56\)
Vậy kl R là sắt(Fe)