Lưu huỳnh (S) cháy trong không khí sinh ra khí sunfurơ (SO2). Phương trình hóa học của phản ứng là S + O2 --------->SO2. Hãy cho biết :
a) Những chất nào tham gia và tạo thành trong phản ứng trên, chất nào là đơn chất, chất nào là hợp chất ? Vì sao?
b) Thể tích khí oxi (đktc) cần dùng để đốt cháy hoàn toàn 1,5 mom nguyên tử lưu huỳnh
c) Khí sunfurơ nặng hay nhẹ hơn không khí ?



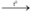 SO
SO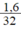 = 0,05 mol.
= 0,05 mol.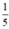 thể tích của không khí nên thể tích không khí cần là
thể tích của không khí nên thể tích không khí cần là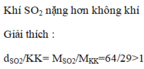


a) Những chất tham gia phản ứng trên: S và O2 vì hai chất trên đều do 1 chất tạo thành.
Những chất tạo thành trong phản ứng trên: SO2 vì chất trên do 2 chất tạo thành.
b) Theo phương trình hoá học, ta có:
Đốt cháy 1 mol S cần dùng 1 mol O2.
Vậy: Đốt cháy 1,5 mol S cần dùng 1,5 mol O2.
=> Thể tích Oxi cần dùng ( đktc ):
VO2= 22,4.n = 22,4.1,5 = 33,6 (l)
c) Ta có:
dSO2/kk=\(\dfrac{64}{29}\)≃ 2,2 => Khí sunfuro nặng hơn không khí 2,2 lần