Đốt cháy 5( g ) hổn hợp cacbon và lưu huỳnh trong bình khí O2 dư, thu được 1,3g hổn hợp sp . Tính VO2 ( đkc ) cần dùng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi nC = a (mol); nS = b (mol)
12a + 32b = 12 (1)
PTHH:
C + O2 -> (t°) CO2
a ---> a ---> a
S + O2 -> (t°) SO2
b ---> b ---> b
44a + 64b = 28 (2)
Từ (1)(2) => a = 0,2 (mol); b = 0,3 (mol)
nO2 = 0,2 + 0,3 = 0,5 (mol)
VO2 = 0,5 . 22,4 = 11,2 (l)

BTKL: \(m_{S+C}+m_{O_2}=m_{SO_2+CO_2}\)
\(\Rightarrow m_{O_2}=15,2-5,6=9,6g\)
\(\Rightarrow n_{O_2}=0,3mol\)
\(\Rightarrow V_{O_2}=0,3\cdot22,4=6,72l\)
\(\Rightarrow V_{kk}=5\cdot6,72=33,6l\)

X gồm: CH4 và C2H4
C2H4 + Br2 => C2H4Br2
mC2H4Br2 = m/M = 37.6/188 = 0.2 (mol)
Theo phương trình ==> nC2H4 = 0.2 (mol)
CH4 + 2O2 => CO2 + 2H2O (1)
C2H4 + 3O2 => 2CO2 + 2H2O (2)
nC2H4 = 0.2 (mol) => nCO2(2) = 0.6 (mol)
VCO2 = 16.8 (l) => nCO2 = 16.8/22.4 = 0.75 (mol)
==> nCO2 (1) = 0.75 - 0.6 = 0.15 (mol)
==> nCH4 = 0.075 (mol)
Ta có: nCH4 = 0.075 (mol), nC2H4 = 0.2 (mol)
===> nhh = 0.275 (mol)
%nCH4 = 27.27%, %nC2H4 = 72.73%

Đáp án D
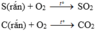
Từ 2 phương trình trên ta thấy số mol khí của chất tham gia phản ứng và sau phản ứng bằng nhau và không phụ thuộc vào lượng C, S => do vậy áp suất của bình sẽ không thay đổi khi ta đưa về nhiệt độ ban đầu

Gọi số mol C, S là a, b
=> 12a + 32b = 7,68
PTHH: C + O2 --to--> CO2
_____a--------------->a
S + O2 --to--> SO2
b--------------->b
=> a + b = \(\dfrac{9,856}{22,4}=0,44\)
=> a = 0,32; b = 0,12
=> \(\left\{{}\begin{matrix}\%C=\dfrac{0,32.12}{7,68}.100\%=50\%\\\%S=\dfrac{0,12.32}{7,68}.100\%=50\%\end{matrix}\right.\)

a) \(n_{SO_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH: S + O2 --to--> SO2
0,5<-0,5<------0,5
=> mS = 0,5.32 = 16(g)
=> \(\left\{{}\begin{matrix}\%m_S=\dfrac{16}{22,2}.100\%=72,07\%\\\%m_P=\dfrac{22,2-16}{22,2}.100\%=27,93\%\end{matrix}\right.\)
b) \(n_P=\dfrac{22,2-16}{31}=0,2\left(mol\right)\)
PTHH: 4P + 5O2 --to--> 2P2O5
0,2-->0,25----->0,1
=> \(V_{O_2}=0,25.22,4=5,6\left(l\right)\)
c)
PTHH: 2KClO3 --to--> 2KCl + 3O2
0,5<-------------------0,75
=> \(m_{KClO_3}=0,5.122,5=61,25\left(g\right)\)
a) PTHH:
\(S+O_2\rightarrow\left(t^o\right)SO_2\\ 4P+5O_2\rightarrow\left(t^o\right)2P_2O_5\)
- Chất khí mùi hắc là SO2
- Chất rắn sau phản ứng có m(g) là P2O5
Đặt: nS=a(mol); nP=b(mol) (a,b>0) (nguyên, dương)
\(\Rightarrow\left\{{}\begin{matrix}32a+31b=22,2\\22,4a=11,2\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,5\\b=0,2\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}\%m_S=\dfrac{0,5.32}{22,2}.100\approx72,072\%\\\%m_P\approx100\%-72,072\%\approx27,928\%\end{matrix}\right.\)
b)
\(n_{O_2}=a+\dfrac{5}{4}b=0,5+\dfrac{5}{4}.0,2=0,75\left(mol\right)\\ \Rightarrow V_{O_2\left(đktc\right)}=0,75.22,4=16,8\left(l\right)\)
c)
\(2KClO_3\rightarrow\left(t^o\right)2KCl+3O_2\\ n_{KClO_3}=\dfrac{2}{3}.n_{O_2}=\dfrac{2.0,75}{3}=0,5\left(mol\right)\\ \Rightarrow m_{KClO_3}=122,5.0,5=61,25\left(g\right)\)

áp dụng định luật bảo toàn khối lượng ta có :
Σmhh + mo2 =ms02 + mco2 <=> 4,4 + 6,4 = mso2 + mco2 <=> mso2 + mco2 = 10,8

Đặt :
nS = x mol
nP = y mol
mhh = 32x + 31y = 10.765 (g) (1)
S + O2 -to-> SO2
4P + 5O2 -to-> 2P2O5
nO2 = x + 1.25y = 0.4 (2)
(1) , (2) :
x = 0.11
y = 0.2625
%mP = 0.2625*31 / 10.765 * 100% = 75.59%
%S = 24.41%
moxit = mSO2 + mP2O5 = 0.11*64 + 0.25/2 * 142 = 24.79(g)
*Sửa đề: Thu được 13g hh sản phẩm
Bảo toàn khối lượng: \(m_{O_2\left(p.ứ\right)}=m_{hỗn.hợp}-\left(m_C+m_S\right)=13-5=8\left(g\right)\)
\(\Rightarrow n_{O_2}=\dfrac{8}{32}=0,25\left(mol\right)\) \(\Rightarrow V_{O_2}=0,25\cdot22,4=5,6\left(l\right)\)