Bài 2: Khi oxi hóa 7,8 gam kali thu được kali oxit.
a. Tính khối lượng kali oxit thu được và thể tích khí oxi cần dùng ở đktc.
b. Tính khối lượng KMnO4 cần dùng để thu được lượng khí oxi dùng cho phản ứng trên.
Bài 3: Dẫn 1,12 lít khí lưu huỳnh đi oxit(đktc) đi qua 5,18gam canxi hiđroxit. Thu được canxi sunfat và nước.
a. Viết PTHH.
b. Khối lượng các chất thu được sau phản ứng.

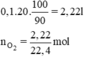
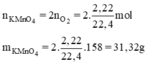

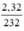 = 0,01 mol.
= 0,01 mol.
Bài 2:
a) nK=7,8/39=0,2(mol)
PTHH: 4K + O2 -to-> 2 K2O
nK2O=2/4 . 0,2=0,1(mol) =>mK2O=94.0,1=0,4(g)
nO2=1/4. 0,2=0,05(mol) => V(O2,đktc)=0,05.22,4=1,12(l)
b) PTHH: 2 KMnO4 -to-> K2MnO4 + MnO2 + O2
nKMnO4= 2.0,05=0,1(mol) => mKMnO4=158.0,1=15,8(g)
Bài 3:
nSO2=1,12/22,4=0,05(mol)
nCa(OH)2=5,18/74=0,07(mol)
Vì 1< nCa(OH)2/nSO2=0,07/0,05=1,4<2
=> Sp thu được là muối trung hòa duy nhất, Ca(OH)2 dư
PTHH: Ca(OH)2 + SO2 -> CaSO3 + H2O (1)
0,05_________0,05_____0,05(mol)
b) mCaSO3=0,05.120=6(g)
mCa(OH)2 (dư)=74. (0,07-0,05)= 1,48(g)