Một hỗn hợp A gồm Ba và Al.
Cho m gam A tác dụng với nước dư, thu được 1,344 lít khí, dung dịch B và một phần không tan C.
Cho 2m gam A tác dụng với dung dịch Ba(OH)2 dư thu được 20,832 lít khí. (Các phản ứng đều xảy ra hoàn toàn, các thể tích khí đo ở điều kiện tiêu chuẩn).
a) Tính khối lượng từng kim loại trong m gam A.
b) Cho 50 ml dung dịch HCl vào dung dịch B. Sau khi phản ứng xong, thu được 0,78 gam kết tủa. Xác định nồng độ mol/lít của dung dịch HCl
em đăng lần thứ ba rồi ạ , mong các CTV làm cho và đề không thiếu hay sai gì ạ


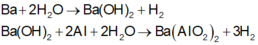
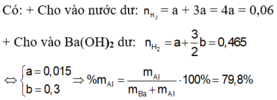

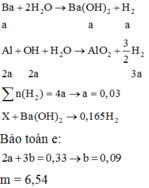

Lần trước em đăng đề thiếu nên mới không làm được nhé em !
a) Đặt x, y lần lượt là số mol Ba,Al trong hỗn hợp A
Cho m gam A + H2O dư
=> Phần không tan C là Al dư
Ba + 2H2O → Ba(OH)2 + H2
x--------------------->x-------->x
2Al + Ba(OH)2 + 2H2O → Ba(AlO2)2 + 3H2
2x<-----x---------------------------->x----------->3x
=>\(n_{H_2}=x+3x=\dfrac{1,344}{22,4}=0,06\) (1)
Cho 2m gam A + Ba(OH)2 dư
=> Số mol Ba,Al lần lượt là 2x; 2y
Vì kiềm dư nên cả 2 kim loại đều tan hết
Ba + 2H2O → Ba(OH)2 + H2
2x------------------->2x-------->2x
2Al + Ba(OH)2 + 2H2O → Ba(AlO2)2 + 3H2
2y----->y-------------------------->y----------->3y
=>\(n_{H_2}=2x+3y=\dfrac{20,832}{22,4}=0,93\) (2)
Từ (1), (2) => x=0,015 (mol) ; y=0,3(mol)
\(\Rightarrow m_{Ba}=0,015.137=2,005\left(mol\right);m_{Al}=0,3.27=8,1\left(g\right)\)
b) Dung dịch B chứa Ba(AlO2)2 : 0,015(mol)
\(n_{Al\left(OH\right)_3}=\dfrac{0,78}{78}=0,01\left(mol\right)\)
TH1: Kết tủa chưa đạt giá trị max và còn Ba(AlO2)2 dư
Ba(AlO2)2 + 2HCl + 2H2O → BaCl2 + 2Al(OH)3
Theo PT: \(n_{HCl}=n_{Al\left(OH\right)_3}=0,01\left(mol\right)\)
=> \(CM_{HCl}=\dfrac{0,01}{0,05}=0,2M\)
TH2: Kết tủa đạt giá trị max và bị HCl dư hòa tan 1 phần
Ba(AlO2)2 + 2HCl + 2H2O → BaCl2 + 2Al(OH)3
0,015-------->0,03----------------------------->0,03
\(n_{Al\left(OH\right)_3\left(bihoatan\right)}=0,03-0,01=0,02\left(mol\right)\)
Al(OH)3 + 3HCl → AlCl3 + 3H2O
0,02-------->0,06
=> \(\Sigma n_{HCl}=0,03+0,06=0,09\left(mol\right)\)
=> \(CM_{HCl}=\dfrac{0,09}{0,05}=1,8M\)
thanks ạ