Hãy viết cấu hình electron: Fe, Fe2+, Fe3+, S, S2-, Rb và Rb+. Biết: ZFe= 26; ZS= 16; ZRb= 37
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án D
26Fe: 1s22s22p63s23p63d64s2
=> Fe3+: 1s22s22p63s23p63d5

Đáp án B
+ Đối với kim loại có cấu hình electron (n - 1)dxnsy, khi tham gia phản ứng sẽ nhường electron ở ns trước sau đó (n - 1)d.
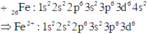

H: 1 s 1 ; Li: 2 s 1 ; Na: 3 s 1 ; K: 4 s 1 ; Rb: 5 s 1 ; Cs: 6 s 1 ; Fr:7 s 1
Nguyên tử của các nguyên tố thuộc nhóm IA chỉ có 1 electron ở lớp ngoài cùng trên phân lớp s (n s 1 ). Trừ hiđro, còn các nguyên tố khác đều có tên là kim loại kiềm. Vì chỉ có 1 electron ở lớp ngoài cùng nên trong các phản ứng hoá học, nguyên tử của các kim loại kiềm có khuynh hướng nhường đi 1 electron để đạt được cấu hình vững bền của các khí hiếm đứng trước. Do đó, các kim loại kiềm chỉ có hoá trị 1.

