Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nHCl=0,6V1 mol; n NaOH=0,4V2 mol
Do dd A có thể hòa tan Al2O3=> HCl hoặc NaOH dư
*TH1: HCl dư
Al2O3+6HCl-> 2AlCl3+3H2O nAl2O3=0,01 mol=> nHCl dư =0,06 mol
nHCl phản ứng= n NaOH=0,4V2 mol=>n HCl dư = 0,6V1-0,4V2=0,06 mol
V1+V2=0,6l
giải hpt ra V1=V2=0,3l
*TH2: NaOH dư
2NaOH+Al2O3-> 2NaAlO2+H20 (3)
n NaOH dư=2nAl2O3=0,02 mol
=>nNaOH dư= 0,4V2-0,6V1=0,02 mol
V1+V2=0,6l
giải hpt ra V1=0,22l, V2=0,38l

a) Mg+ 2H2SO4→ MgSO4+ SO2+ 2H2O
(mol) 0,2 0,4 0,2
nMg=\(\dfrac{m}{M}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
V SO2= n.22,4= 0,2.22,4= 4,48 (lít)
b) Ta có: CM H2SO4= \(\dfrac{n}{V}\)
<=> V H2SO4= \(\dfrac{n}{C_M}\)=\(\dfrac{0,4}{2}=0,2\left(lít\right)\)
Số mol của magie
nMg = \(\dfrac{m_{Mg}}{M_{Mg}}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
Pt : Mg + H2SO4 → MgSO4 + H2\(|\)
1 1 1 1
0,2 0,2 0,2
a) Số mol của khí hidro
nH2 = \(\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
Thể tích của khí hidro
VH2 = nH2 . 22,4
= 0,2 . 22,4
= 4,48 (l)
b) Số mol của axit sunfuric
nH2SO4 = \(\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
Thể tích của dung dịch axit sunfuric đã dùng
CMH2SO4 = \(\dfrac{n}{V}\Rightarrow V=n.C_M=0,2.2=0,4\left(l\right)\)
Chúc bạn học tốt

\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right);n_S=\dfrac{9,6}{32}=0,3\left(mol\right)\)
PTHH: \(Fe+S-^{t^o}\rightarrow FeS\)
Theo đề: 0,2...0,3
Lập tỉ lệ \(\dfrac{0,2}{1}< \dfrac{0,3}{1}\)=> Fe hết. S dư
=> Sau phản ứng hỗn hợp gồm S dư, FeS
=> \(n_{S\left(dư\right)}=0,3-0,2=0,1\left(mol\right)\)
S + H2SO4 → SO2 + H2O
2FeS + 10H2SO4 → Fe2(SO4)3 + 9SO2 + 10H2O
\(\Rightarrow m_{H_2SO_4}=\left(0,1+\dfrac{0,2.10}{2}\right).98=107,8\left(g\right)\)
\(V_{SO_2}=\left(0,1+\dfrac{0,2.9}{2}\right).22,4=22,4\left(l\right)\)
\(n_{Fe_2\left(SO_4\right)_3}=\dfrac{1}{2}n_{FeS}=0,1\left(mol\right)\)
3Ba(OH)2 + Fe2(SO4)3 → 2Fe(OH)3↓ + 3BaSO4↓ (*)
Fe(OH)3 ---to→ Fe2O3 + H2O (**)Theo PT (*) : \(n_{Fe_2\left(SO_4\right)_3}=\dfrac{1}{2}n_{Fe\left(OH\right)_3}=0,05\left(mol\right)\)
Theo PT (**): \(n_{Fe_2O_3}=2n_{Fe\left(OH\right)_3}=0,1\left(mol\right)\)
\(\Rightarrow m_{Fe_2O_3}=0,1.160=16\left(g\right)\)

Gọi số mol của Ba, Al và Mg lần lượt là x, y và z mol
Lượng khí thu được khi cho A vào nước dư ít hơn khi cho A vào xút dư nên khi cho A vào nước dư thì Ba phản ứng hết, Al phản ứng một phần. Khi cho A vào xút dư thì cả Ba và Al đều phản ứng hết.
Cho A tác dụng với nước dư có phản ứng:
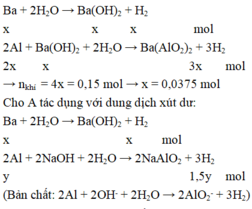

Khối lượng của A là: m = 0,0375.137 + 0,175.27 + 0,1.24 = 12,2625 gam.
⇒ Chọn B

a) Bảo toàn nguyên tố H : \(n_{HCl}.1=2n_{H_2}=0,6\left(mol\right)\)
=> nH2=0,3(mol)
=> \(V_{H_2}=0,3.22,4=6,72\left(l\right)\)
b) Áp dụng định luật bảo toàn khối lượng :
\(m_{ct}=m_{kl}+m_{HCl}-m_{H_2}=10,4+0,6.36,5-0,3.2=31,7\left(g\right)\)

PT: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\) (1)
\(2Fe+6H_2SO_{4\left(đ\right)}\underrightarrow{t^o}Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\) (2)
\(5SO_2+2KMnO_4+2H_2O\rightarrow2MnSO_4+K_2SO_4+2H_2SO_4\) (3)
Ta có: \(n_{H_2}=0,2\left(mol\right)\)
Theo PT (1): \(n_{Fe}=n_{H_2}=0,2\left(mol\right)\)
Theo PT (2): \(n_{SO_2}=\dfrac{3}{2}n_{Fe}=0,3\left(mol\right)\)
\(\Rightarrow V_{SO_2}=0,3.22,4=6,72\left(l\right)\)
Theo PT (3): \(n_{KMnO_4}=\dfrac{2}{5}n_{SO_2}=0,12\left(mol\right)\)
\(\Rightarrow V_{KMnO_4}=\dfrac{0,12}{2}=0,06\left(l\right)\)
Bạn tham khảo nhé!