Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(Fe+S-t^0->FeS\\ n_{Fe}:n_S=\dfrac{11,2}{56}:\dfrac{4,8}{32}=0,2:0,15\Rightarrow Fe:dư\left(0,05mol\right)\\ Fe+2HCl->FeCl_2+H_2\\ FeS+2HCl->FeCl_2+H_2S\\ d_{\dfrac{B}{kk}}=\dfrac{\dfrac{0,05.2+0,15.34}{0,2}}{29}=0,89655\)

\(m_{Fe}=\frac{5,6}{56}=0,1\left(mol\right)\); \(m_S=\frac{1,6}{32}=0,05\left(mol\right)\)
PTHH: Fe + S --> FeS
0,1 0,05
Xét tỉ lệ: \(\frac{0,1}{1}>\frac{0,05}{1}\) => Fe dư, S hết
PTHH: Fe + S --> FeS
0,05 - 0,05 - 0,05 (mol)
\(=>\left\{{}\begin{matrix}n_{FeS}=0,05\left(mol\right)\\n_{Fe\left(dư\right)}=0,1-0,05=0,05\left(mol\right)\end{matrix}\right.\)
PTHH: FeS + 2HCl --> FeCl2 + H2S
0,05 -> 0,1 (mol)
Fe +2HCl --> FeCl2 + H2
0,05 -> 0,1 (mol)
=> \(n_{HCl}=0,1+0,1=0,2\left(mol\right)\)
=> \(V_{HCl}=0,2.1=0,2\left(l\right)\)
MIK NGHĨ ZẬY !!!

nFe = 0,1 mol; nS = 0,05 mol
a) Phương trình phản ứng:
Fe + S → FeS (1)
nFe dư = 0,1 – 0,05 = 0,05 nên hỗn hợp chất rắn A có Fe và FeS.
Fe + 2HCl → FeCl2 + H2↑ (2)
FeS + 2HCl → FeCl2 + H2S↑ (3)
b) Dựa vào phương trình phản ứng (2) và (3), ta có:
nHCl= 0,1 + 0,1 = 0,2 mol
VHCl = 0,2 /1 = 0,2 lít.

nFe = \(\frac{5,6}{56}\) = 0,1 mol; ns = \(\frac{1,6}{32}\) = 0,05 mol.
a) Phương trình hoá học: Fe + S \(\underrightarrow{t^o}\) FeS.
Lúc ban đầu: 0,1 0,05 0 (mol)
Lúc phản ứng: 0,05 0,05 0,05
Sau phản ứng: 0,05 0 0,05
Chất rắn A gồm FeS và Fe dư + HCl?
FeS + 2HCl → FeCl2 + H2S
Phản ứng: 0,05 0,1 0,05 0,05 (mol)
Fe + 2HCl → FeCl2 + H2
Phản ứng: 0,05 0,1 0,05 0,05 (mol).
Số mol HCl tham giá phản ứng = 0,1 + 0,1 = 0,2 mol.
Thể tích dung dịch HCl 1M dùng là: Vdd = \(\frac{n}{C_M}\) = \(\frac{0,2}{1}\) = 0,2 lít.

a)
\(n_{Fe} = \dfrac{5,6}{56} = 0,1(mol)\\ n_S = \dfrac{2,4}{32} = 0,075(mol)\)
Fe + S \(\xrightarrow{t^o}\) FeS
0,075.......0,075,,,,,,0,075...................(mol)
nFe dư = 0,1 - 0,075 = 0,025(mol)
Fe + 2HCl → FeCl2 + H2
0,025.....0,05..........................0,025............(mol)
FeS + 2HCl → FeCl2 + H2S
0,075.........0,15...........................0,075.............(mol)
\(\Rightarrow V_{dd\ HCl} = \dfrac{0,05+0,15}{1} = 0,2(lít)\)
b) VB = (0,025 + 0,075).22,4 = 2,24(lít)

a, Ta có: \(n_{Zn}=\dfrac{19,5}{65}=0,3\left(mol\right)\)
\(n_S=\dfrac{1,6}{32}=0,05\left(mol\right)\)
PT: \(Zn+S\underrightarrow{t^o}ZnS\)
Xét tỉ lệ: \(\dfrac{0,3}{1}>\dfrac{0,05}{1}\), ta được Zn dư.
Theo PT: \(n_{Zn\left(pư\right)}=n_{ZnS}=n_S=0,05\left(mol\right)\)
\(\Rightarrow n_{Zn\left(dư\right)}=0,3-0,05=0,25\left(mol\right)\)
- Chất rắn A gồm Zn dư và ZnS.
PT: \(ZnS+2HCl\rightarrow ZnCl_2+H_2S\)
_____0,05___0,1________________0,05 (mol)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,25____0,5__________0,25 (mol)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{H_2S}=\dfrac{0,05.22,4}{\left(0,05+0,25\right).22,4}.100\%\approx16,67\%\\\%V_{H_2}\approx83,33\%\end{matrix}\right.\)
b, \(V_{HCl}=\dfrac{0,1+0,5}{0,5}=1,2\left(l\right)\)





nFe =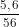 = 0,1 mol; ns =
= 0,1 mol; ns = 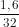 = 0,05 mol.
= 0,05 mol.
a) Phương trình hoá học: Fe + S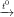 FeS.
FeS.
Lúc ban đầu: 0,1 0,05 0 (mol)
Lúc phản ứng: 0,05 0,05 0,05
Sau phản ứng: 0,05 0 0,05
Chất rắn A gồm FeS và Fe dư + HCl?
FeS + 2HCl → FeCl2 + H2S
Phản ứng: 0,05 0,1 0,05 0,05 (mol)
Fe + 2HCl → FeCl2 + H2
Phản ứng: 0,05 0,1 0,05 0,05 (mol).
Số mol HCl tham giá phản ứng = 0,1 + 0,1 = 0,2 mol.
Thể tích dung dịch HCl 1M dùng là: Vdd =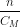 =
= 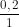 = 0,2 lít.
= 0,2 lít.