Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án C
Đốt 1 mol CxH2y + 10 mol O2 ―t0→ x mol CO2 + y mol H2O + ? mol O2 dư.
Bảo toàn nguyên tố O có nO2 dư = (10 – x – 0,5y) mol.
H2SO4 đặc hấp thụ H2O ⇒ hỗn hợp khí Z gồm CO2 và O2 dư.
dZ/H2 = 19 → MZ = 38 ⇒ nCO2 : nO2 dư = (38 – 32) ÷ (44 – 38) = 1 : 1
⇒ x = 10 – x – 0,5y ⇒ 4x + 2y = 20 ||⇒ x = 4; y = 8.
Vậy, công thức phân tử của X là C4H8. Chọn đáp án C.

Đáp án C
Hướng dẫn M Z - = 19.2 = 18 gam/mol Þ Z gồm CO2 và O2
Áp dụng sơ đồ đường chéo ta có
n C O 2 n C O 2 = 44 - 38 38 - 32 = 1 1
Phương trình phản ứng :
CxHy + (x + y 4 )O2 ® xCO2 + y 2 H2O
bđ: 1 10
pư: 1 ® (x + y 4 ) ® x
spư: 0 10 – (x + y 4 ) x
Þ 10 – (x + y 4 ) = x Þ 40 = 8x + y Þ x = 4 và y = 8

Xét `a<b->H` tính theo `Fe.`
`Fe+S` $\xrightarrow{t^o}$ `FeS`
`0,5a->0,5a->0,5a(mol)`
Có `n_{Fe\ pu}=0,5a(mol)`
`Y` gồm `Fe:0,5a(mol);S:b-0,5a(mol);FeS:0,5a(mol)`
`FeS+2HCl->FeCl_2+H_2S`
`Fe+2HCl->FeCl_2+H_2`
Theo PT: `n_{H_2S}=n_{FeS}=0,5a(mol);n_{H_2}=n_{Fe}=0,5a(mol)`
`->{n_{H_2S}}/{n_{H_2}}={5.2-2}/{34-5.2}=1/3`
``->{0,5a}/{0,5a}=1/3` vô lí.
Xét `a>b->H` tính theo `S.`
`Fe+S` $\xrightarrow{t^o}$ `FeS`
`0,5b←0,5b->0,5b(mol)`
Có `n_{S\ pu}=0,5b(mol)`
`Y` gồm `Fe:a-0,5b(mol);S:0,5b(mol);FeS:0,5b(mol)`
`FeS+2HCl->FeCl_2+H_2S`
`Fe+2HCl->FeCl_2+H_2`
Theo PT: `n_{H_2S}=n_{FeS}=0,5b(mol);n_{H_2}=n_{Fe}=a-0,5b(mol)`
`->{n_{H_2S}}/{n_{H_2}}={5.2-2}/{34-5.2}=1/3`
``->{0,5b}/{a-0,5b}=1/3`
`->1,5b=a-0,5b`
`->a=2b`
`->a:b=2:1`

Đáp án A
Quy về đốt 0,22 mol đipeptit dạng CnH2nN2O3.
Bảo toàn O ||→ có (0,22 × 3 + 1,98 × 2) ÷ 3 = 1,54 mol CO2 = H2O ||→ nH2O trao đổi = 0,14 mol.
→ nE = 0,08 mol → E gồm 0,02 mol Xn và 0,06 mol Y10–n ||→ có 0,02n + 0,06(10 – n) = 0,44 → n = 4.
Lại để ý số Ctrung bình α-amino axit = 1,54 ÷ 0,22 ÷ 2 = 3,5 ||→ ∑nGly = ∑nVal.
Giả sử X4 là (Gly)a(Val)4–a và Y6 là (Gly)b(Val)6–b
→ có phương trình: a + 3b = (4 – a) + 3(6 – b) ||→ a + 3b = 11. Nghiệm nguyên duy nhất a = 2; b = 3.
Theo đó, trong Y có 3Gly và 3Val ||→ tỉ lệ là 1 : 1.

Đáp án A
Trong Y: nX = 0,35 mol; nH2 = 0,07 mol → Trong X: nC2H4 = 0,25 và nC3H6 = 0,1.
- Vì tỉ lệ mol của hai ankan bằng tỉ lệ mol của 2 anken tương ứng ban đầu; mặt khác anken, hiđro tham gia phản ứng và ankan tạo ra đều với số mol như nhau
→ hhZ có 0,07 mol ankan và 0,35 - 0,07 = 0,28 mol anken dư, trong đó:
nC3H6 = 0,7143 x 0,28 = 0,2
→ nC2H4 = 0,02.
nC3H8 = 0,7143 x 0,07 = 0,05
→ nC2H6 = 0,02

Khối lượng muối mỗi phần là 26,1 gam.
Như đã đề cập ở phần lí thuyết, khi nhiệt phân muối nitrat, tùy mức độ hoạt động của kim loại mà muối nitrat kim loại sẽ nhiệt phân từ muối nitrit đến oxit kim loại rồi về kim loại.
Vì thực hiện 2 thí nghiệm ở hai mức nhiệt độ khác nhau thu được kết quả khác nhau nên muối đã nhiệt phân ở các mức khác nhau.
Với thí nghiệm ở nhiệt độ thấp hơn chỉ thu được một khí A nên khí này là O2 và M(NO3)n chỉ nhiệt phân tạo thành muối nitrit M(NO2)n.
Với thí nghiệm ở nhiệt độ cao hơn thu được hỗn hợp khí B, do đó hỗn hợp khí B chứa NO2 và O2. Khi đó M(NO3)n là muối có khả năng nhiệt phân tạo thành oxit kim loại hoặc kim loại.
Các phản ứng xảy ra

Đáp án C.
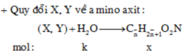
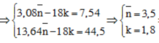
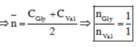
Chọn A