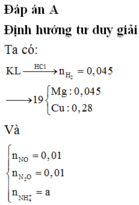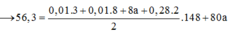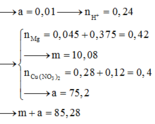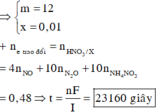Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Vì Mg + dung dịch X → N2O và NO ⇒ X có chứa HNO3.
+ Nhận thấy 0,036 gam hỗn hợp kim loại chính là Ag và Mg.
⇒ X chứa AgNO3 dư và nMg dư = 0,005 mol ⇒ nAg = 0,002 mol
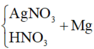
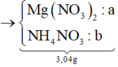
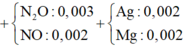
+ PT theo bảo toàn e ta có: 2nMg = nAg + 8nNH4+ + 8nN2O + 3nNO.
Û 2a – 8b = 0,032 (1).
+ PT theo khối lượng muối: 148a + 80b = 3,04 (2).
+ Giải hệ (1) và (2) ⇒ nMg pứ = 0,02 và nNH4NO3 = 0,001.
⇒ Bảo toàn nitơ ta có nHNO3/X = 0,047 mol.
⇒ t = 0,047 × 96500 ÷ 2 = 2267,75s

Đáp án D
Vì Mg + dung dịch X → N2O
và NO ⇒ X có chứa HNO3.
+ Nhận thấy 0,036 gam hỗn hợp
kim loại chính là Ag và Mg.
⇒ X chứa AgNO3 dư và
nMg dư = 0,005 mol
⇒ nAg = 0,002 mol
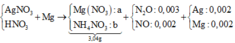
+ PT theo bảo toàn e ta có:
2nMg = nAg + 8nNH4+ + 8nN2O + 3nNO.
Û 2a – 8b = 0,032 (1).
+ PT theo khối lượng muối:
148a + 80b = 3,04 (2).
+ Giải hệ (1) và (2)
⇒ nMg pứ = 0,02 và nNH4NO3 = 0,001.
⇒ Bảo toàn nitơ ta có
nHNO3/X = 0,048 mol.
⇒ t = 0,048 × 96500 ÷ 2 = 2316s

Đáp án D
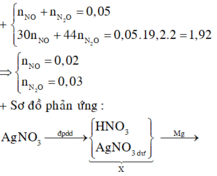
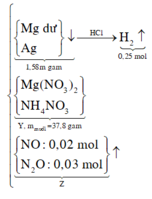
Đặt nNO = x; nN2O = y ⇒ nZ = x + y = 0,005 mol; mZ = 30x + 44y = 0,005 × 19,2 × 2.
||⇒ giải hệ có: x = 0,002 mol; y = 0,003 mol || nMg dư = nH2 = 0,005 mol
⇒ nAg = (0,336 – 0,005 × 24) ÷ 108 = 0,002 mol. Đặt nMg phản ứng = a. Bảo toàn electron:
2nMg phản ứng = 3nNO + 8nN2O + 8nNH4NO3 + nAg ⇒ nNH4NO3 = (0,25a – 0,004) mol
||⇒ mmuối = 148a + 80.(0,25a – 0,004) = 3,04(g) ⇒ a = 0,02 mol. Lại có:
► ne = nH+ = nHNO3 = 4nNO + 10nN2O + 10nNH4NO3 = 0,048 mol ⇒ t = 2316(s)

Chọn đáp án D.
Ghép cụm NO3:
1NO + 2Otrong H2O→ 1NO3
1NO + 5Otrong H2O→ 2NO3
1NH4 + 3Otrong H2O→ 1NO3
→ Gọi số mol NH3NO3 là x mol ta có: ∑nH2O = 3x + 0,02x3 + 0,03x5 = 3x + 0,21
→ Theo bảo toàn nguyên tố H có (6x + 0,42) mol HNO3.
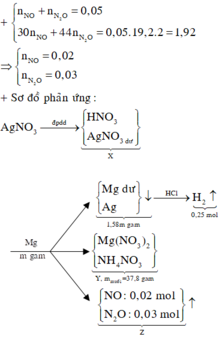
Lại gọi số mol Mg(NO3)2 trong T là y mol → bảo toàn nguyên tố N có (2y -4x -0,34) mol AgNO3.
Bảo toàn khối lượng các nguyên kim loại trong sơ đồ có phương trình:
m + (2y – 4x – 0,34) x108 = 1,58m →0,58m + 432x -192y + 36,72 =0 (1)
Hỗn hợp Y gồm 0,25 mol Mg và (2y -4x -0,34) mol Ag mà khối lượng Y là 1,58m gam
→ phương trình:0,25 x 24 + (2y – 4x – 0,34) x 108 = 1,58m →1,58 + 432x -216y + 30,72 =0 (2)
Biết mT = 37,8 gam → có 148y + 80x = 37,8 (3)
Giải hệ được x = 0,0 mol; y = 0,25 mol và m = 12,0 gam. Thay lại có 0,48 mol HNO3.
→ khi điện phân: ne trao đổi = 0,48 mol → t = 0,48 x 96500 : 2 = 23160 giây