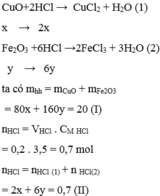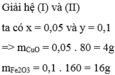Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Cho 16 gam hỗn hợp A gồm CuO và Fe2O3. Tính khối lượng mỗi oxit trong A, biết rằng để hòa tan hết 12 gam A cần vừa đủ 250 ml dung dịch HCl 2M.
Chỗ in đậm là đúng hả cậu ?

Gọi số mol của MgO và Fe2O3 lần lược là x, y.
\(\Rightarrow40x+160y=12\left(1\right)\)
\(MgO\left(x\right)+2HCl\left(2x\right)\rightarrow MgCl_2+H_2O\)
\(Fe_2O_3\left(y\right)+6HCl\left(6y\right)\rightarrow2FeCl_3+3H_2O\)
Ta có: \(n_{HCl}=2.0,25=0,5\left(mol\right)\)
\(\Rightarrow2x+6y=0,5\left(2\right)\)
Từ (1) và (2) ta có hệ: \(\left\{{}\begin{matrix}40x+160y=12\\2x+6y=0,5\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,05\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{MgO}=0,1.40=4\left(g\right)\\m_{Fe_2O_3}=0,05.160=8\left(g\right)\end{matrix}\right.\)

nNaOH=0.01(mol)
2NaOH+SO2->Na2SO3+H2O
0.01 0.005
V=0.112(l)
2)nHCl=0.5(mol)
MgO+2HCl->MgCl2+H2O
x 2x
Fe2O3+6HCl->2FeCl3+3H2O
y 6y
Theo bài ra:40x+160y=12
2x+6y=0.5
x=0.1(mol) mMgO=4(g)
y=0.05(mol) mFe2O3=8(g)

CuO + 2HCl -> CuCl2 + H2O (1)
Fe2O3 + 6HCl -> 2FeCl3 + 3H2O (2)
nHCl=0,2.3,5=0,7(mol)
Đặt nCuO=a
nFe2O3=b
Ta có hệ:
80a+160b=20
2a+6b=0,7
=>a=0,05;b=0,1
mCuO=80.0,05=4(g)
mFe2O3=20-4=16(g)
Theo PTHH 1 và 2 ta có:
nCuCl2=nCuO=0,05(mol)
nFeCl3=2nFe2O3=0,2(mol)
mCuCl2=135.0,05=6,75(g)
mFeCl3=162,5.0,2=32,5(g)
mdd =20+200.1,1=240(g)
C% dd CuCl2=6,72\240 .100%=2,8125%
C% dd FeCl3= 32,5\240 .100%=13,54%

\(a/ZnO+2HCl\rightarrow ZnCl_2+H_2O\\ Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\\ b/n_{HCl}=\dfrac{250.7,3}{100}:36,5=0,5mol\\ n_{ZnO}=a;n_{Fe_2O_3}=b\\ \Rightarrow\left\{{}\begin{matrix}81a+160b=16,1\\2a+6b=0,5\end{matrix}\right.\\ \Rightarrow a=b=0,1mol\\ \%m_{ZnO}=\dfrac{0,1.81}{16,1}\cdot100=50,3\%\\ \%m_{Fe_2O_3}=100-50,3=49,7\%\\ c/C_{\%ZnCl_2}=\dfrac{136.0,1}{16,1+250}\cdot100=5\%\\ C_{\%FeCl_3}=\dfrac{0,1.2.162,5}{16,1+250}=12\%\)

\(n_{HCl}=0,5.1=0,5\left(mol\right)\)
a)
\(CuO+2HCl\rightarrow CuCl_2+H_2O\)
x------->2x
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
y--------->6y
Có hệ: \(\left\{{}\begin{matrix}2x+6y=0,5\\80x+160y=16\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,05\end{matrix}\right.\)
\(m_{CuO}=0,1.80=8\left(g\right)\\ m_{Fe_2O_3}=0,05.160=8\left(g\right)\)
b
\(\%m_{CuO}=\dfrac{0,1.80.100\%}{16}=50\%\\ \%m_{Fe_2O_3}=\dfrac{0,05.160.100\%}{16}=50\%\)

a,\(n_{HCl}=0,5.1=0,5\left(mol\right)\)
PTHH: CuO + 2HCl → CuCl2 + H2O
Mol: x 2x
PTHH: Fe2O3 + 6HCl → 2FeCl3 + 3H2O
Mol: y 6y
Ta có: \(\left\{{}\begin{matrix}80x+160y=16\\2x+6y=0,5\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,05\end{matrix}\right.\)
PTHH: CuO + 2HCl → CuCl2 + H2O
Mol: 0,1 0,2
PTHH: Fe2O3 + 6HCl → 2FeCl3 + 3H2O
Mol: 0,05 0,3
\(\Rightarrow m_{CuO}=0,1.80=8\left(g\right);m_{Fe_2O_3}=16-8=8\left(g\right)\)
b,\(\%m_{CuO}=\dfrac{8.100\%}{16}=50\%;\%m_{Fe_2O_3}=100-50=50\%\)

Gọi $n_{CaO} = a(mol) ; n_{Fe_2O_3} = b(mol) \Rightarrow 56a + 160b = 24,4(1)$
$CaO + 2HCl \to CaCl_2 + H_2O$
$Fe_2O_3 + 6HCl \to 2FeCl_3 + 3H_2O$
$n_{HCl} = 2a + 6b = 0,45. 2= 0,9(2)$
Từ (1)(2) suy ra a = 0,15; b = 0,1
$m_{CaO} = 0,15.56 = 8,4(gam)$