Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án : A
Bảo toàn C và H,.
m = (9:18).2 + 17,6 : 44 . 12 = 5,8

Đáp án A
Crackinh m gam n-butan
→ hhA gồm H2, CH4, C2H6, C3H6, C4H8 và C4H10 dư.
Đốt cháy hhA cũng chính là đốt cháy m gam C4H10.
Đặt nC4H10 = a mol → nCO2 = 4a mol; nH2O = 5a mol.
![]()
→ a = 0,1 mol → m = 0,1 x 58 = 5,8 gam

Đáp án : B
Phương trình phản ứng:
C4H10 => C4H8 + H2 (1)
C4H10 => C3H6 + CH4 (2)
C4H10 => C2H4 + C2H6 (3)
Sau phản ứng còn C4H10 dư
từ (1), (2), (3):
n C4H8 = n H2
n C3H6 = n CH4
n C2H4 = n C2H6
và n C4H8 + n C3H6 + n C2H4 = n H2 + n CH4 + n C2H6 = n C4H10 đã bị cracking.
n anken bị dung dịch Br2 giữ lại = 35 - 20 = 15 mol --> n C4H10 dư = 20 - 15 = 5 mol
=> n C4H10 ban đầu = 5 + 15 = 20 mol
=> hiệu suất phản ứng = 15 x100%/20 = 75%

Đáp án : D
Bảo toàn nguyên tố của một chất trước và sau phản ứng không quan trọng trung gian .
Ban đầu là C4H10 và cuối cùng là CO2 ; H2O .
Bảo toàn Nguyên tố C : 4nC4H10 = nCO2 => nCO2 = 4 mol => m = 176 g
“Vì C4H10 có 4C => 4nC4H10 ; CO2 có 1C => nCO2”
Bảo toàn nguyên tố H : 10nC4H10 = 2nH2O => nH2O = 5 mol => m = 90 g

Đáp án : A
Do tỉ lệ thể tích bằng tỉ lệ số mol, coi 40l = 40mol, 56l = 56mol
Do cracking nên không thêm chất bên ngoài vào, vậy lượng chênh lệch trước và sau phản ứng chính là lượng butan phản ứng có số mol: 56 - 40 = 16 mol
=> H = 16/40 = 40%

Đáp án A
Áp dụng định luật bảo toàn nguyên tố:
![]()
Khi cho T qua dung dịch nước brom thì C2H4, C2H4, C4H8, C4H6 phản ứng với brom.
![]() (1)
(1)
![]() (2)
(2)
Từ (1) và (2) có
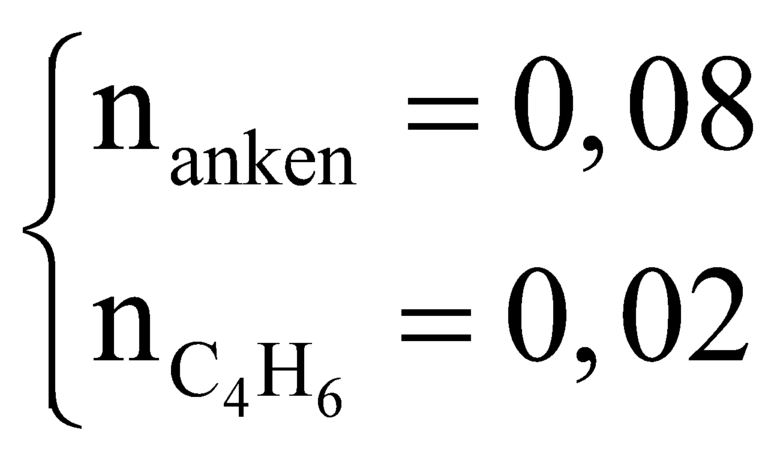
![]()

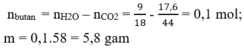
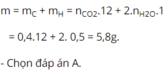


Đốt cháy A cũng giống như đốt cháy lượng C4H10 ban đầu
Bảo toàn nguyên tố C: nC4H10 ban đầu = ¼ nCO2 = 0,1 mol
⇒ m = 0,1.58 = 5,8
Đáp án A.