Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Nhận thấy Mg2+ và H+ không thể tồn tại cùng với CO32-
→Dung dịch A chứa K+, NH4+, CO32- và ion âm An-
Theo định luật bảo toàn điện tích: 0,15+ 0,25=0,15.2+ n.nAn-
→ n.nAn-= 0,1 mol → Anion còn lại trong dung dịch A là Cl-
→Dung dịch A chứa K+, NH4+, CO32- và Cl-
→mchất rắn khan= 0,15.39 + 0,25.18+ 0,15.60 + 0,1.35,5= 22,9 gam
Dung dịch B chứa H+, Mg2+, SO42- và NO3-
Chú ý khi cô cạn thì axit HNO3 (0,2 mol) sẽ bay hơi cùng nước
→mchất rắn khan= mMg2++ mSO4(2-)+ mNO3- dư
= 0,1.24+ 96.0,075+ 0,05.62=12,7 gam

Đáp án B
nCO2= 3,36 : 22,4 = 0,15 (mol);
nNaOH = 0,2 ; nKOH = 0,1 (mol) => ∑ nOH- = 0,3 (mol)
Ta có: nOH-/ nCO2 = 0,3/ 0,15 = 2 => chỉ tạo muối trung hòa
CO2 + 2OH- → CO32- + H2O
0,15 0,3 → 0,15
Vậy dd X gồm : K+, Na+ ; CO32- : 0,15 (mol)
Dd X + Ba(OH)2: 0,2 (mol) có phản ứng
Ba2+ + CO32- → BaCO3↓
0,15← 0,15 →0,15 (mol)
=> mBaCO3 = 0,15. 197 = 29,55 (g)

Đáp án A
n N a 2 C O 3 n N a H C O 3 = 0 , 2 0 , 4 = 1 2
Ta có ( 2 n C O 3 2 - + n H C O 3 - ) = 0 , 8 > n H + = 0 , 2 ⇒ H + hết
Khi cho từ từ A vào B thì C O 3 2 - và H C O 3 - sẽ đồng thời phản ứng với axit.
Vì vậy giả sử nếu C O 3 2 - phản ứng hết x mol thì H C O 3 - sẽ phản ứng 1 lượng đúng bằng tỉ lệ mol trong dung dịch của 2 chất là 2x mol.
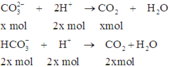
Do H+ hết nên tính theo H+ ta có: 4x = 0,2
![]()

Đáp án C
n Al 3+ + 2 n Fe 2+ + n Na+ = 2 n SO4 2- + n Cl-
=> 2a + b = 0.8 (1)
m muối = m Al 3++ m Fe 2+ + m Na+ + m SO4 2- + m Cl- = 51,6 g
=> 96 a + 35,5 b = 35 ,9 g (2)
Giải (1) và (2 ) ta có a = 0,3 , b = 0,2



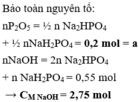


Chọn A