Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(a.n_{CaCl_2}=0,1\left(mol\right)\\ CaCl_2+2AgNO_3\rightarrow Ca\left(NO_3\right)_2+2AgCl\\ n_{AgCl}=2n_{CaCl_2}=0,2\left(mol\right)\\ \Rightarrow m_{AgCl}=0,2.143,5=28,7\left(g\right)\\ b.n_{Ca\left(NO_3\right)_2}=n_{CaCl_2}=0,1\left(mol\right)\\ \Rightarrow CM_{CaCl_2}=\dfrac{0,1}{0,1}=1M\)

Đề bài này cả 2 kim loại tác dụng với lại dd HCl nhưng chỉ cho 1 dữ kiện -> Xem lại đề bài!

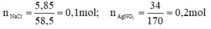
a) Phương trình hóa học của phản ứng:
NaCl + AgNO3 → AgCl↓ + NaNO3
Theo pt: nAgNO3 pư = nAgCl = nNaCl = 0,1 mol
b) Vdd = 300 + 200 = 500 ml
nAgNO3 dư = 0,2 – 0, 1 = 0,1 mol; nNaNO3 = nNaCl = 0,1 mol
CM(NaNO3) = CM(AgNO3) = 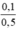 = 0,2 mol/l.
= 0,2 mol/l.

nNaCl = = 0,1 mol;
=
= 0,2 mol
a) Phương trình hóa học của phản ứng:
NaCl + AgNO3 → AgCl↓ + NaNO3
0,1 mol 0,1 mol 0,1 mol 0,1 mol
mAgCl = 143,5 x 0,1 = 14,35g
b) Vdd = 300 + 200 = 500 ml
= 0,2 - 0,1 = 0,1 mol
=
=
= 0,2 mol/l
\(n_{NaCl}=\frac{5,85}{58,5}=0,1\left(mol\right)\)
\(n_{AgNO_3}=\frac{34}{170}=0,2\left(mol\right)\)
\(NaCl+AgNO_3->AgCl+NaNO_3\) (1)
vì \(\frac{0,1}{1}< \frac{0,2}{1}\) => \(AgNO_3dư\)
theo (1) \(n_{AgCl}=n_{NaCl}=0,1\left(mol\right)\)
=> \(m_{AgCl}=143,5.0,1=14,35\left(g\right)\)
b, 300ml=0,3l , 200ml = 0,2 l
\(V_{dd}=0,3+0,2=0,5\left(l\right)\)
theo (1) \(n_{AgNO_3\left(pư\right)}=n_{NaCl}=0,1\left(mol\right)\)
=> \(n_{AgNO_3\left(dư\right)}=0,2-0,1=0,1\left(mol\right)\)
\(C_{M\left(NaNO_3\right)}=\frac{0,1}{0,5}=0,2M\)

PTHH: \(Fe_2O_3+HCl\rightarrow FeCl_3+3H_2O\)
\(n_{Fe_2O_3}=\dfrac{8}{160}=0,05\left(mol\right)\)
a, Bảo toàn nguyên tố Fe:
\(n_{FeCl_3}=n_{Fe}=2n_{Fe_2O_3}=2.0,05=0,1\left(mol\right)\)
\(\Rightarrow m_{FeCl_3}=162,5.0,1=16,25\left(g\right)\)
b, Bảo toàn nguyên tố Cl:
\(n_{HCl}=n_{Cl}=3n_{FeCl_3}=3.0,1=0,3\left(mol\right)\)
\(\Rightarrow V_{ddHCl}=\dfrac{n_{HCl}}{C_M}=\dfrac{0,3}{0,5}=0,6\left(l\right)\)
c, \(C_{M_{FeCl_3}}=\dfrac{n_{FeCl_3}}{V_{ddFeCl_3}}=\dfrac{0,1}{0,6}=0,17M\)
Mk gửi bạn nhé
Đáp án:
a. 16,25g
b. 0,6l
c. 0,05M
Giải thích các bước giải:
Fe2O3+6HCl → 2FeCl3 + 3H2O
0,05 0,3 0,1
nFe2O3= 8/160= 0,05 mol
a. mFeCl3= 0,1. 162,5= 16,25g
b. VHCl= 0,3/0,5 = 0,6l
c. CMFeCl3 = 0,1/0,5= 0,05M

nAgNO3= 0,5x1= 0,5 mol
nHCl=0,3x2=0,6 mol
Pt AgNO3 + HCl = AgCl(kt) + HNO3
n 0,5 0,6
=> dung dịch sau phản ứng gồm HNO3 và HCl dư(AgCl kt nhé)
CM HNO3 = 0,5/(0,5+0,3) = 0,625M
CM HCl dư = (0,6-0,5)/(0,5+0,3) = 0,125M
mdd = 1,2x500 + 1,5x300 = 1050g
C% HNO3 = 3%
C% HCl=0,347%

Đáp án C
![]() = 0,8 mol
= 0,8 mol
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
0,8 → ![]() = 0,72 (mol)
= 0,72 (mol)
Vkhí = 0,72.22,4 = 16,128 (lit)
nNaOH = 2 (mol)
Cl2 + 2NaOH → NaCl + NaClO + H2O
0,72 2 → 0,72 0,72 (mol)
do NaOH dư, tính theo Cl2
Dung dịch sau phản ứng: nNaCl = nNaClO = 0,72 (mol)
nNaOH dư = 0,56 (mol)
CNaCl = CNaClO = 1,44M, CNaOH = 1,12M

Đáp án D
nNaCl =0,1 mol, nAgNO3 = 0,2 mol
NaCl + AgNO3 → AgCl + NaNO3
0,1 → 0,1 0,1 (mol)
Vdd = 300 + 200 = 500 ml
![]() (dư) = 0,2 - 0,1 =0, 1 (mol)
(dư) = 0,2 - 0,1 =0, 1 (mol)
![]() = 0,1 mol
= 0,1 mol
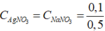 = 0,2 M
= 0,2 M

\(a) n_{Fe_2O_3} = \dfrac{8}{160} = 0,05(mol)\\ Fe_2O_3 + 6HCl \to 2FeCl_3 + 3H_2O\\ n_{FeCl_3} = 2n_{Fe_2O_3} = 0,1(mol)\\ m_{FeCl_3} = 0,1.162,5 = 16,25(gam)\\ b) n_{HCl} = 6n_{Fe_2O_3} = 0,05.6 = 0,3(mol)\\ V_{dd\ HCl} = \dfrac{0,3}{0,5} = 0,6(lít)\\ c) C_{M_{FeCl_3}} = \dfrac{0,1}{0,5} = 0,2M\)


nKCl = 0,1 . 1 = 0,1 (mol)
nAgNO3 = 0,2 . 1 = 0,2 (mol)
PTHH: AgNO3 + KCl -> AgCl + KNO3
LTL: 0,1 < 0,2 => AgNO3 dư
nAgNO3 (p/ư) = nAgCl = nKNO3 = 0,1 (mol)
nAgNO3 (dư) = 0,2 - 0,1 = 0,1 (mol)
Vdd (sau p/ư) = 0,1 + 0,2 = 0,3 (l)
CMAgNO3 = 0,1/0,3 = 0,33M
CMAgCl = 0,1/0,3 = 0,33M
CMKNO3 = 0,1/0,3 = 0,33M