hòa tan hoàn toàn 5,6g iron (Fe) trong 1 lượng vừa đủ dung dịch HCl IM
a) viết phương trình phản ứng
b) tính thể tích H2 thu được sau phản ứng. Biết phản ứng xảy ra ở điều kiện chuẩn.
c) tính thể tích dung dịch HCl cần dùng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

$n_{Fe}=\dfrac{2,24}{56}=0,04(mol)$
$a,PTHH:Fe+2HCl\to FeCl_2+H_2$
$b,$ Theo PT: $n_{H_2}=n_{Fe}=0,04(mol)$
$\Rightarrow V_{H_2}=0,04.22,4=0,896(l)$

a. \(n_{Zn}=\dfrac{6.5}{65}=0,1\left(mol\right)\)
PTHH : Zn + 2HCl -> ZnCl2 + H2
0,1 0,2 0,1
b. \(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
c. \(m_{HCl}=0,2.36,5=7,3\left(g\right)\)
\(n_{Zn}=\dfrac{6,5}{65}=0,1mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,2 0,1
\(V_{H_2}=0,1\cdot22,4=2,24l\)
\(m_{HCl}=0,2\cdot36,5=7,3g\)

\(n_{Zn}=\dfrac{26}{65}=0.4\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(0.4.......0.8....................0.4\)
\(m_{HCl}=0.8\cdot36.5=29.2\left(g\right)\)
\(V_{H_2}=0.4\cdot22.4=8.96\left(l\right)\)

a, PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
b, Ta có: \(n_{Zn}=\dfrac{32,5}{65}=0,5\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Zn}=0,5\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,5.22,4=11,2\left(l\right)\)
c, Theo PT: \(n_{ZnCl_2}=n_{Zn}=0,5\left(mol\right)\)
\(\Rightarrow m_{ZnCl_2}=0,5.136=68\left(g\right)\)

Đáp án A
Hỗn hợp rắn gồm Al, Al2O3, Fe với n Fe = 2 n Al 2 O 3 . Chia thành 2 phần không bằng nhau:
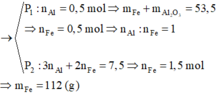

\(n_{Fe}=\dfrac{5.6}{56}=0.1\left(mol\right)\)
\(n_{HCl}=\dfrac{10.95}{36.5}=0.3\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Lập tỉ lệ :
\(\dfrac{0.2}{1}>\dfrac{0.3}{2}\Rightarrow Fedư\)
Khi đó :
\(n_{FeCl_2}=n_{H_2}=\dfrac{1}{2}\cdot n_{HCl}=\dfrac{1}{2}\cdot0.3=0.15\left(mol\right)\)
\(m_{FeCl_2}=0.15\cdot127=19.05\left(g\right)\)
\(V_{H_2}=0.15\cdot22.4=3.36\left(l\right)\)
\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\\ n_{HCl}=\dfrac{10,95}{36,5}=0,3\left(mol\right)\\ PTHH:Fe+2HCl\rightarrow FeCl_2+H_2\\ Vì:\dfrac{0,1}{1}< \dfrac{0,3}{2}\\ \Rightarrow HCldư\\ \Rightarrow n_{FeCl_2}=n_{Fe}=n_{H_2}=0,1\left(mol\right)\\ \Rightarrow m_{FeCl_2}=127.0,1=12,7\left(g\right)\\ V_{H_2\left(đktc\right)}=0,1.22,4=2,24\left(l\right)\)

Bài 3 : Trích mẫu thử :
Cho dung dịch BaCl2 vào 2 mẫu thử :
+ Chất nào xuất hiện kết tủa trắng không tan trong axit : H2SO4
Pt : \(BaCl_2+H_2SO_4\rightarrow BaSO_4+2HCl\)
Không hiện tượng : HCl
Chúc bạn học tốt
Bài 2 :
\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
Pt : \(Fe+H_2SO_4\rightarrow FeSO_4+H_2|\)
1 1 1 1
0,2 0,2 0,2 0,2
a) \(n_{H2SO4}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
\(V_{ddH2SO4}=\dfrac{0,2}{1}=0,2\left(l\right)\)
b) \(n_{H2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,2.22,4=4,48\left(l\right)\)
c) \(n_{FeSO4}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
'\(C_{M_{FeSO4}}=\dfrac{0,2}{0,2}=1\left(M\right)\)
Chúc bạn học tốt

\(n_{HCl}=0,2.2=0,4\left(mol\right)\\ a.Zn+2HCl\rightarrow ZnCl_2+H_2\\ b.0,2........0,4.......0,2.......0,2\left(mol\right)\\ m=m_{Zn}=0,2.65=13\left(g\right)\\ c.m_{ZnCl_2}=136.0,2=27,2\left(g\right)\\ d.V_{H_2\left(đktc\right)}=0,2.22,4=4,48\left(l\right)\)
a, \(Fe+2HCl\rightarrow FeCl_2+H_2\)
b, \(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Fe}=0,1\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,1.24,79=2,479\left(l\right)\)
c, \(n_{HCl}=2n_{Fe}=0,2\left(mol\right)\Rightarrow V_{HCl}=\dfrac{0,2}{1}=0,2\left(l\right)\)