người ta lấy a (g) hh gồm Mg và MgO cho vào 400 ml dd HCl x M (vừa đủ ) được 2,24 (l) khí H2 ở DKTC và ddB đem cô cạn dd B được 28,5 g muối khan .tìm các giá trị của a và x
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đề là a g hh nha bạn
Mg+2HCl--->MgCl2+H2
MgO+2HCl---->MgCl2+H2O
Ta có
n H2=2,24/22,4=0,1(mol)
Theo pthh1
n Mg=n H2=0,1(mol)
m Mg=0,1.24=2,4(g)
n MgCl2 ở pt1 =n H2 =0,1(mol)
m MgCl2=0,1.95=9,5(g)
m muối ở pt2 =28,5-9,5=19(g)
n MgCl2=19.95=0,2(mol)
Theo pthh2
n MgO=n MgCl2=0,2(mol0
m MgO=0,2.40=8(g)
a=m hh=8+2,4=10,4(g)
Theo pthh1
n HCl=2n H2=0,2(mol)
Theo pthh2
n HCl=2n MgCl2=0,4(mol)
\(\sum nHCl=0,2+0,4=0,6\left(mol\right)\)
x=0,6/0,4=1,5(M)
Ngắn gọn hơn bài Dương nhé:
Mg+2HCl\(\rightarrow\)MgCl2+H2 (1)
MgO+2HCl\(\rightarrow\)MgCl2+H2O (2)
nH2=\(\frac{2,24}{22,4}\)=0,1 mol
\(\rightarrow\) nMg=0,1 mol, nMgCl2 (1)=0,1 mol
\(\rightarrow\)mMgCl2(1)=0,1.95=9,5g
\(\rightarrow\) mMgCl2(2)=28,5-9,5=19g
\(\rightarrow\) nMgCl2(2)=nMgO=19:95=0,2 mol
Ta có:
x gam hh tpu= mMg+mMgO=0,1.24+0,2.95=21,4g
CM HCl=(0,1.2+0,2.2)/0,4=1,5M

a)Gọi x,y lần lượt là số mol của Al, Fe trong hỗn hợp ban đầu (x,y>0)
Sau phản ứng hỗn hợp muối khan gồm: \(\left\{{}\begin{matrix}AlCl_3:x\left(mol\right)\\FeCl_2:y\left(mol\right)\end{matrix}\right.\)
Ta có hệ phương trình: \(\left\{{}\begin{matrix}27x+56y=13,9\\133,5x+127y=38\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x\approx0,0896\\y\approx0,205\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,0896\cdot27\cdot100\%}{13,9}\approx17,4\%\\\%m_{Fe}=\dfrac{0,205\cdot56\cdot100\%}{13,9}\approx82,6\%\end{matrix}\right.\)
Theo Bảo toàn nguyên tố Cl, H ta có:\(n_{H_2}=\dfrac{n_{HCl}}{2}=\dfrac{3n_{AlCl_3}+2n_{FeCl_2}}{2}\\ =\dfrac{3\cdot0,0896+2\cdot0,205}{2}=0,3394mol\\ \Rightarrow V_{H_2}=0,3394\cdot22,4\approx7,6l\)

$n_{HCl} = 0,8.0,5 = 0,4(mol) ; n_{H_2SO_4} = 0,6(mol) ;n_{H_2} = 0,2(mol)$
$n_{H(trong\ axit)} = 0,4 + 0,6.2 = 1,6(mol)$
Bảo toàn H : $n_{H_2O} = \dfrac{n_{H(trong\ axit)} - 2n_{H_2} }{2} = 0,6(mol)$
Bảo toàn khối lượng :
$m = 88,7 + 0,6.18 + 0,2.2 - 0,4.36,5 - 0,6.98 = 26,5(gam)$

a)Gọi : \(\left\{{}\begin{matrix}n_{Mg}=a\left(mol\right)\\n_{MgO}=b\left(mol\right)\end{matrix}\right.\)⇒ 24a + 40b = 8,8(1)
\(Mg + 2HCl \to MgCl_2 + H_2\\ MgO + 2HCl \to MgCl_2 + H_2O\)
Theo PTHH :
\(n_{MgCl_2} = a + b = \dfrac{28,5}{95} = 0,3(2)\)
Từ (1)(2) suy ra: a = 0,2 ; b = 0,1
Vậy :
\(m_{Mg} = 0,2.24 = 4,8(gam) ; m_{MgO} = 0,1.40 = 4(gam)\\ \%m_{Mg} = \dfrac{4,8}{8,8}.100\% = 54,54\%\\ \%m_{MgO} = 100\% -54,54\% = 45,45\%\)
b)
\(n_{HCl} = 2n_{MgCl_2} = 0,3.2 = 0,6(mol)\\ C\%_{HCl} = \dfrac{0,6.36,5}{200}.100\% = 10,95\%\)

HD:
4Mg + 10HNO3 \(\rightarrow\) 4Mg(NO3)2 + N2O + 5H2O
0,5 0,1 mol
Theo phản ứng trên thì Mg dư 0,1 mol (vì số mol Mg = 4 lần số mol N2O = 0,4 mol, ban đầu Mg có 0,5 mol).
Sau khi cô cạn dung dịch thu được muối Mg(NO3)2 có số mol là 0,4 mol nên m = 0,4.148 = 59,2 g.
Số mol HNO3 đã phản ứng = 10.0,1 = 1,0 mol nên V = 1/2 = 0,5 lít = 500 ml.

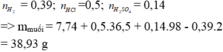

`Mg+2HCl->MgCl_2 +H_2 \uparrow`
`0,1` `0,2` `0,1` `0,1` `(mol)`
`MgO+2HCl->MgCl_2 +H_2 O`
`0,2` `0,4` `0,2` `(mol)`
`n_[H_2]=[2,24]/[22,4]=0,1(mol)`
`n_[MgCl_2(MgO)]=[28,5-0,1.95]/95=0,2(mol)`
`m_[hh]=0,1.24+0,2.40=10,4(g)`
`C_[M_[HCl]]=[0,2+0,4]/[0,4]=1,5(M)`
PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(MgO+2HCl\rightarrow MgCl_2+H_2O\)
Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Theo PT: \(n_{Mg}=n_{H_2}=0,1\left(mol\right)\)
\(n_{MgCl_2}=\dfrac{28,5}{95}=0,3\left(mol\right)\)
Theo PT: \(n_{MgCl_2}=n_{Mg}+n_{MgO}\Rightarrow n_{MgO}=0,2\left(mol\right)\)
\(\Rightarrow a=m_{Mg}+m_{MgO}=0,1.24+0,2.40=10,4\left(g\right)\)
\(n_{HCl}=2n_{Mg}+2n_{MgO}=0,6\left(mol\right)\Rightarrow C_{M_{HCl}}=\dfrac{0,6}{0,4}=1,5\left(M\right)\)