Khi đốt cháy 1 lít hợp chất hữu cơ a cần 5 lít khi oxi. sau phản ứng thu được 3 lít khí co2 và 4 lít hơi nước. xác định công thức phân tử của a, biết thế tích các khí đo ở cùng điều kiện nhiệt độ và áp suất.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


VC = 3 lit; V H = 8
→ V O = 0 vì VO ban đầu = 5.2 = 10 lit = VO sau phản ứng = 2*VC+ V H
Công thức tổng quát : CxHy ta có x:y = 3:8 → công thức của X là C3H8.
VC = VCO2 = 3 (l)
VH = 2 . VH2O = 2 . 4 = 8 (l)
VO (trong oxi) = 5 . 2 = 10 (l)
VO (sau p/ư) = 4 . 2 + 3 = 10 (l)
So sánh: 10 = 10 => trong X chỉ có H và C
CTPT: CxHy
=> x : y = 3 : 8
Vậy X là C3H8

\(nCO2=nC=\dfrac{1.76}{44}=0.04mol\)
\(nH2O=\dfrac{1}{2}nH=0.05\Rightarrow nH=0.1mol\)
\(nNH3=nN=0.02mol\)
\(nO=\dfrac{mX-mC-mN-mH}{16}=\dfrac{1.5-0.04\times12-0.02\times14-0.1\times1}{16}=0.04mol\)
C:H:N:O = 2:5:1:2
=> Công thức đơn giản nhất: (C2H5NO2)n
\(MX=\dfrac{1.5}{0.02}=75\)
=> n = 1 => C2H5NO2

Ta có: \(n_{O_2}=\dfrac{2,856}{22,4}=0,1275\left(mol\right)\)
\(\dfrac{V_{CO_2}}{V_{H_2O}}=\dfrac{4}{3}\Rightarrow\dfrac{n_{CO_2}}{n_{H_2O}}=\dfrac{4}{3}\)
Gọi: nCO2 = 4x (mol) ⇒ nH2O = 3x (mol)
Theo ĐLBT KL, có: mA + mO2 = mCO2 + mH2O
⇒ 2,82 + 0,1275.32 = 4x.44 + 3x.18
⇒ x = 0,03
⇒ nCO2 = 0,03.4 = 0,12 (mol) = nC
nH2O = 0,03.3 = 0,09 (mol) ⇒ nH = 0,09.2 = 0,18 (mol)
Ta có: mC + mH = 0,12.12 + 0,18.1 = 1,62 (g) < 2,82 (g)
→ A chứa C, H và O.
⇒ mO = 2,82 - 1,62 = 1,2 (g) \(\Rightarrow n_O=\dfrac{1,2}{16}=0,075\left(mol\right)\)
Gọi CTPT của A là CxHyOz
⇒ x:y:z = 0,12:0,18:0,075 = 8:12:5
→ CTPT của A có dạng là (C8H12O5)n (n nguyên dương)
Mà: \(M_A< 29.7=203\left(g/mol\right)\)
\(\Rightarrow\left(12.8+12.1+16.5\right)n< 203\)
⇒ n < 1,08 ⇒ n = 1
Vậy: CTPT của A là C8H12O5.

Đáp án B
| Thuốc thử |
Mẫu thử |
Hiện tượng |
| Dung dịch NaHCO3 |
X |
Có bọt khí |
| Dung dịch AgNO3/NH3,t0 |
X |
Kết tủa Ag trắng sáng |
| Y |
Kết tủa Ag trắng sáng |
|
| Z |
Không hiện tượng |
|
| Cu(OH)2/OH- |
Y |
Dung dịch xanh lam |
| Z |
Dung dịch xanh lam |
|
| T |
Dung dịch tím |
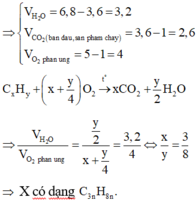
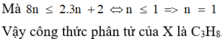

a)
n CO2 = 6,6/44 = 0,15(mol) => n C = n CO2 = 0,15(mol)
n H2O = 5,4/18 = 0,3(mol) => n H = 2n H2O = 0,6(mol)
=> n O = (4,8 - 0,15.12 - 0,6)/16 = 0,15(mol)
Ta có :
n C : n H : n O = 0,15: 0,6 : 0,15 = 1 : 4 : 1
=> CTP của A là (CH4O)n
M A = (12 + 4 + 16)n = 3,2/(2,24/22,4) = 32
=> n = 1
Vậy CTPT của A là CH4O
b)
$2CH_3OH + 2Na \to 2CH_3ONa + H_2$
n CH3OH = n CO2 = 0,15(mol)
=> n H2 = 1/2 n CH3OH = 0,075(mol)
=> V H2 = 0,075.22,4 = 1,68(lít)


Ở cùng điều kiện nhiệt độ và áp suất, tỉ lệ số mol cũng là tỉ lệ thể tích.
BTNT O, có: \(V_{O\left(trongA\right)}+2V_{O_2}=2V_{CO_2}+V_{H_2O}\Rightarrow V_{O\left(trongA\right)}=0\)
Vậy: A chỉ gồm C và H.
Gọi CTPT của A là CxHy.
\(\Rightarrow\left\{{}\begin{matrix}x=\dfrac{n_{CO_2}}{n_A}=3\\y=\dfrac{2n_{H_2O}}{n_A}=8\end{matrix}\right.\)
Vậy: CTPT cần tìm là C3H8