Câu 7: Dùng khí CO để khử hoàn toàn 20 gam một hỗn hợp (hỗn hợp Y) gồm CuO và Fe2O3 ở nhiệt độ cao. Sau phản ứng, thu được chất rắn chỉ là các kim loại, lượng kim loại này được cho phản ứng với dd H2SO4 loãng (lấy dư), thì thấy có 3,2 gam một kim loại màu đỏ không tan.
a) Tính % khối lượng các chất có trong hỗn hợp Y ?
b) Nếu dùng khí sản phẩm ở các phản ứng khử Y, cho đi qua dung dịch Ca(OH)2 dư thì thu được bao nhiêu gam kết tủa. Biết hiệu suất của phản ứng này chỉ đạt 80% ?


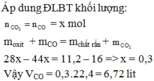

a)
Kim loại màu đỏ không tan là Cu
\(n_{Cu}=\dfrac{3,2}{64}=0,05\left(mol\right)\)
PTHH: CuO + CO --to--> Cu + CO2
0,05<-----------0,05-->0,05
=> mCuO = 0,05.80 = 4 (g)
=> \(\left\{{}\begin{matrix}\%m_{CuO}=\dfrac{4}{20}.100\%=20\%\\\%m_{Fe_2O_3}=100\%-20\%=80\%\end{matrix}\right.\)
b)
\(m_{Fe_2O_3}=\dfrac{20-4}{160}=0,1\left(mol\right)\)
PTHH: Fe2O3 + 3CO --to--> 2Fe + 3CO2
0,1----------------------->0,3
=> \(n_{CO_2}=0,05+0,3=0,35\left(mol\right)\)
PTHH: Ca(OH)2 + CO2 --> CaCO3 + H2O
0,35---->0,35
=> \(m_{CaCO_3\left(lý.thuyết\right)}=0,35.100=35\left(g\right)\Rightarrow m_{CaCO_3\left(tt\right)}=\dfrac{35.80}{100}=28\left(g\right)\)