Cho khí CO dư đi qua 13,92 gam một oxit sắt đã nung nóng, sau khi phản ứng thu được khí A và chất rắn B. Hòa tan hoàn toàn B trong dung dịch H2SO4 loãng dư, sau phản ứng hoàn toàn thu được 4,032 lít H2 (đktc). Xác định công thức hóa học của oxit sắt?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(V_{H_2\left(đktc\right)}=\dfrac{4,032}{22,4}=0,18\left(mol\right)\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
1 : 1 (mol)
0,18 : 0,18 (mol)
\(yCO+Fe_xO_y\rightarrow^{t^0}xFe+yCO_2\uparrow\)
1 : x (mol)
\(\dfrac{0,18}{x}\) 0,18 (mol)
\(M_{Fe_xO_y}=\dfrac{m}{n}=\dfrac{13,92}{\dfrac{0,18}{x}}=\dfrac{232}{3}x\)
\(\Rightarrow56x+16y=\dfrac{232}{3}x\)
\(\Rightarrow16y=\dfrac{64}{3}x\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{16}{\dfrac{64}{3}}=\dfrac{3}{4}\Rightarrow x=3;y=4\)
-Vậy CTHH của oxit sắt là Fe3O4

Chọn đáp án A
Quy A về Cu, Al, Fe và O || [O] + H2SO4 → SO42– + H2O ⇒ nO = nH2SO4 = 0,17 mol.
H2 + [O] → H2O (trừ Al2O3) ⇒ nAl2O3 = (0,17 - 0,08)/3 = 0,03 mol ⇒ nAl = 0,06 mol.
||► Rắn gồm 0,03 mol Al2O3 và Fe2O3 ⇒ nFe2O3 = (6,66 - 0,03 × 102)/160 = 0,0225 mol
⇒ nFe = 0,045 mol ⇒ nCu = (8,14 - 0,06 × 27 - 0,045 × 56 - 0,17 × 16)/64 = 0,02 mol.
⇒ nO/oxit sắt = 0,17 - 0,09 - 0,02 = 0,06 mo ⇒ Fe : O = 0,045 : 0,06 = 3 : 4 ⇒ Fe3O4
⇒ moxit sắt = 0,015 × 232 = 3,48(g) ⇒ chọn A.

Đáp án A
Quy hỗn hợp X chứa hai chất: FeO xmol và Fe2O3 y mol
Cho X+ khí CO→Chất rắn Y + khí Z chứa CO, CO2
CO2+ Ca(OH)2 → CaCO3+ H2O
Có: nCO2= nCaCO3= 0,04 mol
Cho Y + H2SO4 đặc nóng dư thu được nSO2=0,045 mol
- Quá trình cho e:
FeO → Fe3++ 1e
x x mol
C+2 → C+4+ 2e
0,04 0,08 mol
- Quá trình nhận electron:
S+6+ 2e → SO2
0,09← 0,045 mol
Theo định luật bảo toàn electron:
ne cho= ne nhận → x+0,08 = 0,09→ x= 0,01mol
Muối thu được sau phản ứng là Fe2(SO4)3
→ nFe2(SO4)3= 18/400= 0,045 mol
Bảo toàn nguyên tố Fe ta có:
x+ 2y= 0,045.2→ y= 0,04 mol
→ m= mFeO + mFe2O3=72x + 160y= 72.0,01+ 160.0,04= 7,12 gam

Đáp án B
Sau khi hỗn hợp X bị CO lấy
đi 1 phần oxi ⇒ Chất rắn Y.
+ Đặt nFe/Y = a và nO/Y = b ta có:
PT bảo toàn electron:
3a – 2b = 2nSO2 = 0,09 mol (1)
PT theo muối Fe2(SO4)3:
200a = 18 (2)
+ Giải hệ (1) và (2) ta có:
a = b = 0,09 mol
⇒ mY = 0,09(56+16) = 6,48 gam.
+ Mà nO bị lấy đi bởi CO = nCaCO3 = 0,04 mol
⇒ nX = mY + mO bị lấy đi
= 6,48 + 0,04×16 = 7,12 gam

Sau khi hỗn hợp X bị CO lấy đi 1 phần oxi ⇒ Chất rắn Y.
+ Đặt nFe/Y = a và nO/Y = b ta có:
PT bảo toàn electron: 3a – 2b = 2nSO2 = 0,09 mol (1)
PT theo muối Fe2(SO4)3: 200a = 18 (2)
+ Giải hệ (1) và (2) ta có: a = b = 0,09 mol
⇒ mY = 0,09×(56+16) = 6,48 gam.
+ Mà nO bị lấy đi bởi CO = nCaCO3 = 0,04 mol
⇒ nX = mY + mO bị lấy đi = 6,48 + 0,04×16 = 7,12 gam
Đáp án B

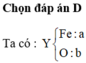
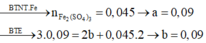

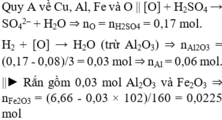
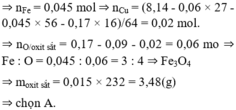
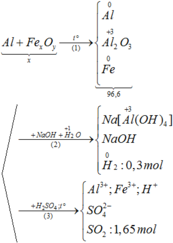
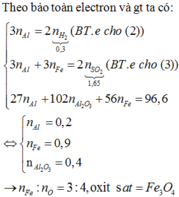

\(n_{H_2}=\dfrac{4,032}{22,4}=0,18\left(mol\right)\)
PTHH: Fe + H2SO4 ---> FeSO4 + H2
0,18 <------------------------ 0,18
\(\rightarrow n_O=\dfrac{13,92-0,18.56}{16}=0,24\left(mol\right)\)
CTHH: FexOy
=> x : y = 0,18 : 0,24 = 3 : 4
CTHH Fe3O4