Dẫn 8,96 lít khí CO2 (đktc) vào 200g dung dịch Ba(OH)2 25,65% thấy tạo thành m (g) ↓ . Tìm m ?
Giúp mình với ạ ☘
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có:
n CO2 = 0,3 ( mol )
n Ca(OH)2 = 0,5 ( mol )
PTHH
CO2 + Ca(OH)2 ====> CaCO3 + H2O
0,3-------0,3------------------0,3
theo pthh: n CaCO3 = n CO2 = 0,3 ( mol )
=> m CaCO3 = 30 ( g )

Giải thích:
Số mol CO2 là 0,4 mol
Số mol Ca(OH)2 là 0,3 mol
Ta có 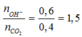 → tạo 2 muối CO32- và muối HCO3-
→ tạo 2 muối CO32- và muối HCO3-
Bảo toàn số mol C ta có ![]() =0,4 mol
=0,4 mol
Bảo toàn điện tích ta có ![]() =0,6 mol
=0,6 mol
Giải được CO32- : 0,2 mol → CaCO3: 0,2 mol → m=20g
Đáp án B

tham khảo
nCO2=5,622,4=0,25(mol);nCa(OH)2=1.0,15=0,15(mol)
PTHH: CO2 + Ca(OH)2 → CaCO3 + H2O
Mol: 0,15 0,15
Tỉ lệ:0,251>0,1510,251>0,151 ⇒ CO2 dư,Ca(OH)2 pứ hết
⇒m=mCaCO3=0,15.100=15(g)
\(n_{CO_2}=\dfrac{5,6}{22,4}=0,25mol\\ n_{BaCO_3}=\dfrac{20}{197}=0,1mol\\ Vì.n_{CO_2}>n_{BaCO_3}\\ pư.tạo.2.muối\\ CO_2+Ba\left(OH\right)_2\rightarrow BaCO_3+H_2O\)
0,1 0,1 0,1 0,1
\(CO_2+Ba\left(OH\right)_2\rightarrow Ba\left(HCO_3\right)_2\)
0,15 0,15 0,15
\(C_{M_X}=C_{M_{Ba\left(OH\right)_2}}=\dfrac{0,1+0,15}{0,15}=\dfrac{5}{3}M\)

Đáp án C
n CO2 = 0,4 mol , n KOH = 0,12 mol , n Ba(OH)2 = 0,24 mol
=> n OH- = 0,24 .2 + 0,12 = 0,6 mol
CO2 + OH- → HCO3-
0,4 0,6 => 0,4 , n OH-dư = 0,2 mol
HCO3- + OH-→ CO32- + H2O
0,4 0,2 => 0,2 mol , dư HCO3-
Ba2+ + CO32- → BaCO3
0,24 0,2 => 0,2 mol
=> m BaCO3 = 39,4 g

nCO2 = \(\dfrac{1,12}{22,4}\)=0,05 mol , nNaOH = 0,5.0,125=0,0625 mol
T=\(\dfrac{nNaOH}{nCO_2}\)= 1,25 => tạo 2 muối \(\left\{{}\begin{matrix}Na_2CO_3\\NaHCO_3\end{matrix}\right.\)
PTHH
CO2 + 2NaOH --> Na2CO3 + H2O
CO2 + NaOH --> NaHCO3
Gọi số mol Na2CO3 và NaHCO3 thu được lần lượt là x và y mol ta có hệ pt :
\(\left\{{}\begin{matrix}2x+y=0,0625\\x+y=0,05\end{matrix}\right.\)=> x = 0,0125 mol và y = 0,0375 mol
=> mNa2CO3 = 0,0125.106 = 1,325 gam
mNaHCO3 = 0,0375 .84 =3,15 gam

n CO2 = 5,6/22,4 = 0,25(mol)
n Ba(OH)2 = 0,2.1 = 0,2(mol)
Ta có :
1 < n Ba(OH)2 / n CO2 = 0,25/ 0,2 = 1,25 < 2 nên chất tạo thành gồm BaCO3, Ba(HCO3)2
Chọn đáp án C
\(n_{CO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\\ n_{Ba\left(OH\right)_2}=\dfrac{200.25,65\%}{171}=0,3\left(mol\right)\\ Vì:0,5< \dfrac{n_{Ba\left(OH\right)_2}}{n_{CO_2}}=\dfrac{0,3}{0,4}=0,75< 1\\ \Rightarrow Sp:\left\{{}\begin{matrix}BaCO_3:a\left(mol\right)\\Ba\left(HCO_3\right)_2:b\left(mol\right)\end{matrix}\right.\\\Rightarrow \left\{{}\begin{matrix}a+b=0,3\\a+2b=0,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\\ \Rightarrow m_{\downarrow}=m_{BaCO_3}=197.0,2=39,4\left(g\right)\)