Làm Giúp Mk vs ....... Thak Trc Na :) :) :) :v
Câu 4. Hoà tan m gam hỗn hợp Na 2 CO 3 và KHCO 3 vào nước để được 400 ml dung dịch X. Cho từ từ 150 ml
dung dịch HCl 1M vào dung dịch X, thu được dung dịch Y và 1,008 lít khí (đktc). Cho Y tác dụng với
Ba(OH) 2 dư, thu được 29,55 gam kết tủa. Giá trị của m là
A. 10,60.
B. 20,13.
C. 11,13.
D. 13,20.
Câu 5. Hai cốc đựng dung dịch HCl đặt trên hai đĩa cân X, Y, cân ở trạng thái...
Đọc tiếp
Làm Giúp Mk vs ....... Thak Trc Na :) :) :) :v
Câu 4. Hoà tan m gam hỗn hợp Na 2 CO 3 và KHCO 3 vào nước để được 400 ml dung dịch X. Cho từ từ 150 ml
dung dịch HCl 1M vào dung dịch X, thu được dung dịch Y và 1,008 lít khí (đktc). Cho Y tác dụng với
Ba(OH) 2 dư, thu được 29,55 gam kết tủa. Giá trị của m là
A. 10,60.
B. 20,13.
C. 11,13.
D. 13,20.
Câu 5. Hai cốc đựng dung dịch HCl đặt trên hai đĩa cân X, Y, cân ở trạng thái cân bằng. Cho 5 gam CaCO 3
vào cốc X và 4,784 gam M 2 CO 3 (M là kim loại kiềm) vào cốc Y. Sau khi hai muối đã tan hoàn toàn, cân trở lại
vị trí thăng bằng. Kim loại M là
A. K.
B. Cs
C. Li
D. Na
Câu 6. Cho dung dịch NaOH dư vào 100 ml dung dịch X chứa đồng thời Ba(HCO 3 ) 2 0,5M và BaCl 2 0,4M thì
thu được m gam kết tủa. Giá trị của m là
A. 9,85.
B. 19,7.
C. 14,775.
D. 17,73.
Câu 7. Cho từ từ dung dịch chứa 0,2 mol HCl vào dung dịch chứa m gam hỗn hợp X gồm Na 2 CO 3 , KHCO 3 thì
thấy có 0,1 mol khí CO 2 thoát ra. Cho dung dịch Ca(OH) 2 dư vào m / 2 gam hỗn hợp X như trên thấy có 15 gam
kết tủa. Giá trị của m là
A. 31,20.
B. 30,60.
C. 39,40.
D. 19,70.
Câu 8. Cho 100 ml dung dịch chứa hỗn hợp Ba(OH) 2 1M và KOH 2M vào 100 ml dung dịch chứa hỗn hợp
NaHCO 3 2M và NH 4 HCO 3 1M. Sau khi phản ứng xẩy ra hoàn toàn, đun nóng hỗn hợp sau phản ứng cho khí
thoát ra hết thì khối lượng dung dịch sau phản ứng giảm bao nhiêu gam so với tổng khối lượng hai dung dịch
tham gia phản ứng? (biết nước bay hơi không đáng kể).
A. 19,7 gam.
B. 12,5 gam.
C. 25,0 gam.
D. 21,4 gam.
Câu 9. Hấp thụ hoàn toàn 4,48 lít CO 2 (đktc) vào 200ml dung dịch chứa Na 2 CO 3 0,5M và NaOH 0,75M thu
được dung dịch X. Cho dung dịch BaCl 2 dư vào dung dịch X thu được kết tủa có khối lượng là
A. 19,7 gam.
B. 39,4 gam
C. 29,55 gam
D. 9,85 gam.
Câu 10. Trên hai đĩa cân đã thăng bằng, đặt hai cốc bằng nhau: Cho vào cốc bên trái 12 gam Mg; cho vào cốc
bên phải 26,94 gam MgCO 3 , cân mất thăng bằng. Muốn cân trở lại thăng bằng như cũ phải thêm vào cốc Mg
bao nhiêu gam dung dịch HCl 14,6% ?
A. 16 gam.
B. 14 gam.
C. 15 gam.
D. 17 gam.


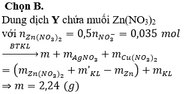
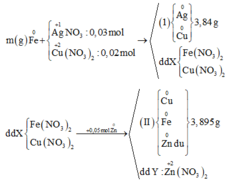

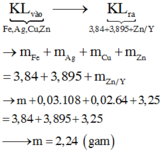

Đáp án A
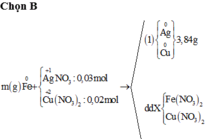
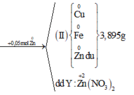
↔ 0,05 mol => cuối cùng Y cho 0,035 mol Z n ( N O 3 ) 2
Bảo toàn khối lượng lần 1: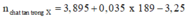 = 7,26 gam
= 7,26 gam
Bảo toàn khối lượng lần 2: => m = 7,26 + 3,84 - 0,03.170 - 0,02.188 = 2,240 gam