Cho 0,81 gam Al và 2,8 gam Fe tác dụng với 200 ml dung dịch X chứa AgNO3 và Cu(NO3)2. Sau khi phản ứng xảy ra hoàn toàn thu được dung dịch Y và 8,12 gam hỗn hợp 3 kim loại. Cho 8,12 gam hỗn hợp 3 kim loại này tác dụng với dung dịch HCl dư. Kết thúc phản ứng thấy thoát ra 0,672 lít khí H2 (đktc). Nồng độ mol của AgNO3 và Cu(NO3)2 lần lượt là:
A. 0,15M và 0,25M
B. 0,10M và 0,20M
C. 0,25M và 0,15M
D. 0,25M và 0,25M


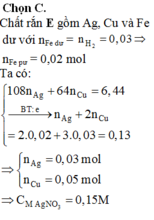

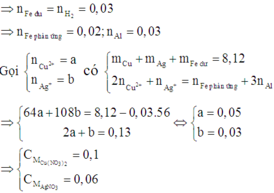

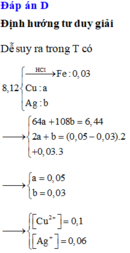
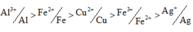
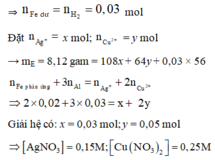

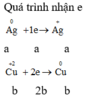


Đáp án A
Sau phản ứng thu được 3 kim loại => Fe còn dư; Al, AgNO3 và Cu(NO3)2 đều phản ứng hết; 3 kim loại thu được gồm Ag, Cu và Fe dư.
Đặt số mol của AgNO3 và Cu(NO3)2 lần lượt là a, b